Gram leke temeli, malzemeleri, teknikleri ve kullanımları
Gram leke Tanısal mikrobiyolojide en basit ve en kullanışlı boyama tekniğidir. Bu teknik, hücre duvarının bileşimine göre, Gram pozitif ve Gram negatif olarak bakterileri sınıflandırmayı başarabilen 1884 yılında Danimarkalı doktor Hans Christian Gram tarafından oluşturuldu..
Bu teknik, 1921 yılında reaktifleri dengelemek ve lekenin kalitesini arttırmak için Hucker tarafından belirli modifikasyonlara tabi tutulmuştur, böylece Gram boyası ayrıca Gram Hucker olarak da bilinir..
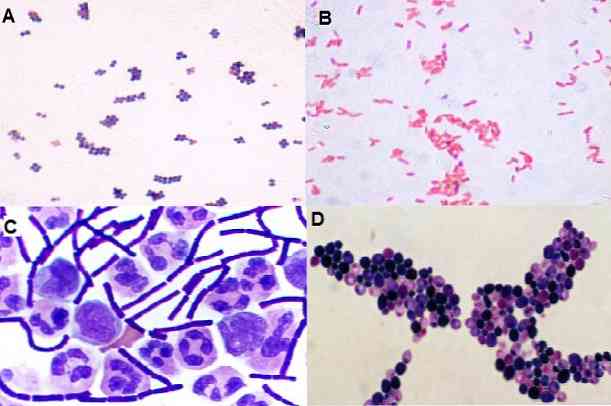
Bu teknikle, mikroorganizmaların sahip oldukları, yani kokci, basil, kokobakilli, pleomorfik, filamentli olup olmadıklarını gözlemlemek de mümkündür. Uzayda dağılmasının yanı sıra: kümede, zincirde, izole edilmiş, çiftler halinde, tetrads vb..
Bakteriyel bir enfeksiyondan şüphelenildiğinde, alınan örneklerin çoğu bir lam üzerine yayılmalı ve mikroskop altında incelenmek üzere Gram ile lekelenmelidir..
Gram raporu, doktora mahsulün son sonucunu almadan önce ne tür bir mikroorganizmanın enfeksiyonun nedeni olabileceği konusunda rehberlik edecektir..
Bazı durumlarda, hastanın ömrü çok tehlikelidir, bu nedenle doktorlar, mikroorganizmanın tanımlanmasını beklerken ampirik bir tedavi için Gram raporuna acilen ihtiyaç duyuyorlar..
Örneğin, eğer Gram beyin omurilik sıvısında Gram pozitif kokların olduğunu ortaya çıkarırsa, doktor ilk tedaviyi, bu tür bakterileri ortadan kaldıran antibiyotiklerle yönlendirir, bunun için oluşturulan protokollere göre..
Nihai sonuç izole edilmiş mikroorganizmanın adı ve ilgili antibiyogramı ile birlikte geldiğinde, doktor tedaviyi değiştirip değiştirmeyeceğini değerlendirecektir. Bu karar, mikroorganizmanın aldığı antibiyotiklere duyarlılığı ve hastanın evrimi üzerine yapılan çalışmalara göre verilecek..
indeks
- 1 Vakfı
- 2 Malzemeler
- 3 Boyalar ve reaktiflerin hazırlanması
- 3.1 Kristal menekşe çözümü
- 3.2 İyodo-Lugol
- 3.3 Ağartma
- 3.4 Kontrast
- 4 Reaktiflerin depolanması
- 5 Renklendirilecek numunenin yayılmasının hazırlanması
- 5.1 -Doğrudan örnekler numunesi
- 5.2 - Ürün mahsulü
- 6 Tekniği
- 7 Yardımcı Program
- 8 Yaygın hatalar
- 9 Kaynaklar
vakıf
Bu, 4 temel adım sunan bir tekniktir: boyama, mordanla fiksasyon, renk değişimi ve zıtlık. Bu nedenle, bu teknik bakterileri renklendirmeye ek olarak, aynı zamanda onları ayırt eder.
Kristal menekşe kullanılan ilk renklendiricidir. Peptidoglikan için bir afiniteye sahiptir ve mor mevcut tüm bakterileri boyar, daha sonra lugol yerleştirilir, bir mordan görevi görür, yani hücre içinde kristal mor-iyot - ribonükleer proteinlerin çözünmeyen komplekslerinin oluşumunu tetikler.
Kalın bir peptidoglikan duvarına sahip olan gram pozitif bakteriler daha kompleksler (kristal menekşe-iyot) oluşturur, bu nedenle boyayı tutarlar.
Aynı zamanda, Gram-pozitif bakteri duvarının, oksitleyici ajanlar (Lugol) için yüksek bir afinite gösteren daha fazla miktarda doymamış asit içerdiğini de etkiler..
Bu arada, Gram negatif bakteriler ince bir peptidoglikan tabakasına sahiptir ve bu da bakterileri Gram pozitif bakterilere göre daha az karmaşık hale getirir..
Daha sonra Gram pozitif ve Gram negatif bakterilerin farklı davranış gösterdiği solma basamağı geliyor.
Gram negatif bakteriler, hücre duvarının bir parçası olan lipopolisakkaritler bakımından zengin bir dış zarı içerir. Yağlar, alkol asetonuyla temas yoluyla imha edilir, böylece dış membran kararsızlaştırılır, menekşe kristali serbest bırakılır..
Bu, daha sonra safranin veya bazik fuchsin ile kırmızı renk alarak karşı karşıya kalmasıdır..
Gram-pozitif bakteri durumunda, renklenmeye karşı direnç gösterirler çünkü ağartıcı gözenekleri kapatmaya etki eder ve kristal mor / iyot kompleksinin kaçmasını önler.
Bu nedenle, menekşe kristali ile renklenme kararlıdır ve safranin veya fuchsin için yer yoktur. Bu nedenle, bu bakteriler yoğun mavi ya da mor lekeler.
malzemeler
Gram boyama seti şunlardan oluşur:
- Menekşe kristali
- lugol
- Aseton alkol
- Safranin veya bazik fuchsin
Boyaların ve reaktiflerin hazırlanması
Kristal menekşe çözümü
Çözüm A:
Menekşe kristali -2 gr
Etil alkol% 95 -20cc
Çözüm b:
Amonyum oksalat -0.8 gr
Damıtılmış su-80 cc
Menekşe kristalinin son hazırlanması için, 1:10 çözelti damıtılmış suyla seyreltilmeli ve 4 kısım B çözeltisiyle karıştırılmalıdır. Karışım kullanımdan önce 24 saat bekletilir. Bir kağıt filtre kullanılarak amber lekelenmesi için bir şişeye süzülür..
Günlük kullanılacak miktar, damlalıklı amber bir şişeye aktarılır..
İyodo-lugol
Her bileşiğin belirtilen miktarını aşağıdaki gibi tartın ve ölçün:
İyodo Kristalleri - 1gr
Potasyum İyodür - 2gr
Damıtılmış su -300 cc
Potasyum iyodür suda azar azar çözünür ve sonra iyot eklenir. Solüsyon amber renkli bir şişeye traş edildi.
Günlük kullanılacak miktar, damlalıklı daha küçük bir amber şişeye aktarılır..
ağartma
% 95 etil alkol -50 mi
Aseton - 50 ml
Eşit kısımda hazırlanır. Kapak iyi, buharlaşma eğilimi gösterir.
Damlalıklı bir şişeye yerleştirin.
Bu hazırlık 5-10 sn orta sürede renk değişikliği sağlar ve en çok önerilen.
Yeni başlayanlar, renk bozulmalarının 10 ila 30 saniye arasında yavaş olduğu yerlerde sadece% 95 etil alkol kullanmayı tercih ediyor.
En tecrübeli olanları saf aseton kullanabilirken, renk değişimi 1 ile 5 saniye arasında çok hızlı gerçekleşir..
kontrast
Safranin stok çözümü
Safranina -2,5 gr
Etil alkol% 95 - 100 cc
Tartıldıktan sonra, belirtilen safranin miktarı 100 cc etil alkol içinde% 95'e erir.
Çalışan safranin çözeltisi stok çözeltiden hazırlanır..
Bunu yapmak için, 10 cc stok solüsyon ölçün, 100 ml tamamlamak için 90 cc damıtılmış su ekleyin.
Günlük kullanılacak miktarın damlalıklı kehribar şişesine aktarılması tavsiye edilir..
Bazı anaeroblar gibi Gram-Hucker boyası ile zayıf bir şekilde Gram negatif lekelenen mikroorganizmalar, Legionella sp, Campylobacter sp ve Brucella sp, Kopeloff tarafından Gram-Hucker boyama, Gram-Kopeloff boyama olarak adlandırılan değişiklik kullanılırsa, daha iyi lekelenebilirler.
Bu teknik safranin boyasını bazik fuchsin ile değiştirir. Bu modifikasyon ile yukarıda belirtilen mikroorganizmaları etkili bir şekilde renklendirmek mümkündür.
Reaktiflerin depolanması
Hazırlanan boyalar oda sıcaklığında saklanmalıdır.
Renge yayılan örneklerin hazırlanması
Bir örnek en az 10 içermelidir5 Bir smeardaki mikroorganizmanın gözlenmesinden önce mikroorganizmalar muhtemeldir. Doğrudan veya numune veya kültürlerden katı veya sıvı ortamlarda yayılabilir..
Mevcut yapıların daha iyi görselleştirilmesi için formalar düzgün, iyi dağılmış ve çok kalın olmamalıdır.
-Doğrudan örneklerin gramı
Santrifüj olmadan idrar gram
İdrar karıştırılır ve slayt üzerine 10 ul yerleştirilir. En az bir bakteri / daldırma alanının gözlemlenmesi bir enfeksiyon olduğunu gösterir.
Bu, kültürün yaklaşık 100.000 CFU / ml'den fazla olacağı anlamına gelir (105 CFU / mL) idrar vakalarının% 85'inde.
Bu yöntem, 100.000 CFU altındaki koloniler için yararlı değildir.
LCR Gram
CSF santrifüjlenmeli, süpernatan uzaklaştırılmalı ve pelet bir lam üzerine yayılmalıdır. Bu sıvı normal şartlar altında sterildir; Bakterilerin gözlenmesi enfeksiyonu gösterir.
Solunum örnekleri gram
Balgam Gram, bronşiyal veya bronkoalveolar lavaj, çeşitli mikroorganizmalar bulunmasına rağmen, gözlenen hücrelerin türünün faydalı olmasının yanı sıra, teşhiste her zaman yol gösterici olacaktır..
Balgam durumunda, smear, numunenin en cüruflu bölümleriyle hazırlanmalıdır..
Dışkı Gram
Teşhis değeri bulunmadığından bu tip numunelere Gram yapılması önerilmez..
-Gram bitkileri
Biri sıvı bitkilerden diğeri katı bitkilerden iki şekilde yapılabilirler.
Sıvı ürünler
Sıvı kültürlerden son derece basittir; çakmağın altında, bulanık et suyunun birkaç kızağı alınır ve materyali düzgün bir şekilde dağıtmak için merkezden çevreye doğru dairesel hareketler veren temiz ve kuru bir sürgü üzerine yerleştirilirler.
Havada kendiliğinden kurumaya bırakılır. Kuruduktan sonra, malzeme tabakaya ısı ile sabitlenir. Bunun için, bir kelepçe yardımıyla, tabaka 3 malzemeyi yakmamaya özen göstererek Bunsen yakıcının alevi boyunca 4 kez geçirilir.
Yaprak soğumaya bırakılır ve renklendirme köprüsü üzerine yerleştirilir.
Katı ürünler
Gram boyama için katı bir kültürden bir uzatma yapmak için aşağıdakileri yapın:
Alınacak kolonileri seçmeden önce, slayt yaklaşık olarak steril fizyolojik tuzlu su çözeltisinden iki damla koyarak hazırlanmalıdır..
Orijinal kültür plakası birkaç farklı tipte kolonilere sahipse, Gramı gerçekleştirmek için her birinin izole bir kolonisi seçilecektir. Her koloni, daha önce slayt üzerine yerleştirilmiş salin çözeltisinde çözünmesi için platin ilmeğiyle alınacaktır..
Dairesel hareketler merkezden çevreye, koloniyi slayt üzerinde homojen olarak dağıtmak için verilir..
Havada kendiliğinden kurumaya bırakılır. Kuruduktan sonra tabaka yukarıda açıklandığı gibi (slaytı çakmakla yakma) ısıyla sabitlenir, malzemeyi yakmamaya özen gösterin.
Bu prosedür her farklı koloni tipi ile yapılmalıdır. Bir kağıda gözlenenlerin sırası not edilmelidir, örneğin:
Koloni 1: Sarı beta-hemolitik koloni: Kümelerde gram pozitif koklar gözlendi
Koloni 2: Krem kolonisi, hemolizsiz: Gram negatif kokobakilli gözlendi.
Her bir sayfa neyi gözlemlediğimizi bilmek için etiketlenmelidir..
teknik
Gram boyama tekniğinin uygulanması son derece basittir ve nispeten ucuzdur ve bir mikrobiyoloji laboratuvarında kaçırılamaz.
Aynısı şu şekilde yapılır:
- Smear'i renkli köprüye ısı ve yer ile sabitleyin.
- Tabaka 1 dakika boyunca tamamen mor cam ile kaplanmıştır..
- Su ile yıkayınız. Kurutmayın
- Plakayı Lugol çözeltisiyle örtün, 1 dakika bekleyin. Su ile yıkayınız. Kurutmayın.
- Aseton alkolde hafifçe çalkalanarak 5-10 saniye karıştırın. Ya da levhayı dik bir pozisyonda yerleştirin ve kalan mor cam sürüklenene kadar renk giderici ajanın damlacıklarını yüzeye bırakın. Aşmayın.
- Su ile yıkayınız. Kurutmayın.
- Renkli köprüdeki levhayı değiştirin ve safranin (Gram-Hucker) ile 30 saniye boyunca veya temel fuchsin (Gram-Kopeloff) ile 1 dakika boyunca örtün.
- Su ile yıkayın
- Dikey havada kendiliğinden kurumaya bırakın.
Kuruduktan sonra, optik mikroskopta 100X hedefi altında gözlemlemek için 1 damla daldırma yağı yerleştirin.
yarar
Bu teknik, çoğu bakterinin morfotipintiyal farklılıklarını ayırt etmeyi sağlar.
Mayalar da bu renk ile ayırt edilir. Kristal menekşe alıyorlar, yani Gram pozitif boyaıyorlar.
Öte yandan, Gram pozitif spor oluşturucu basil ayırt edilebilir, burada sporlar iyi boyanmasa da, endosporun oluşturulduğu basil içerisinde açık bir alan gözlenir. Sporları kullanmak için, Shaeffer-Fulton gibi diğer teknikler kullanılır.
Bu lekenin tüm bakteri türlerini renklendirmek için hizmet etmediği, yani lekelenmenin çalışmadığı durumlar olduğu belirtilmelidir..
Bu durumda, hücre duvarı olmayan bakterilerden söz edilebilir. Örneğin: cins Mycoplasma, sferoplastlar, Ureaplasma, L formları ve protoplastlar.
Ayrıca Mikobakteriler gibi mikolik asitler bakımından zengin çeperli duvarları ve Chlamydias ve Rickettsias gibi hücre içi bakterileri de kötü şekilde boyar..
Ayrıca çoğu spirochetal bakteri lekelemek için verimsizdir.
Gram pozitif ve Gram negatif olarak aynı örnekte gözlemlenebilen aynı cinsin bakterileri vardır. Bu olduğunda, besin, sıcaklık, pH veya elektrolit konsantrasyonundaki değişmelerden kaynaklanabilecek değişken Gram boyası denir..
Yaygın hatalar
Aşırı ağartıcı
Renk değişikliği basamağında abartmak, hatalı gram negatif mikroorganizmaların gözlenmesine neden olabilir.
Daldırma yağı eklemek için yeterli kuruma süresi için beklemeyin:
Bu hata, mevcut yapıların izlenmesini zorlaştıran yağlı misellerin oluşumuna neden olur. Bu, yağın smear içindeki su moleküllerini birleştirdiğinde gerçekleşir..
Reaktiflerin sırasını ters çevirin:
Bunun gibi bir hata Gram negatif bakterilerin mor, yani yanlış Gram pozitif olarak mor görünmesine neden olur..
Eski mahsulleri kullanın (katı veya sıvı):
Gram pozitif bakterilerin Gram negatif (yanlış Gram negatif) lekelenmesine neden olabilir. Bu, eski kültürlerde ölü veya bozulmuş bakteri olma ihtimalinin muhtemel olması ve bu koşullar altında bakterilerin menekşe kristalini tutmaması muhtemeldir..
Çok eski Lugol çözümü kullanın:
Zamanla lugol özelliklerini kaybeder ve rengi kaybolur. Zaten dejenere edilmiş reaktif kullanılırsa, kristal viyole iyi sabitlenmeyecektir, bu nedenle yanlış Gram negatif olan mikroorganizmaların görselleştirilmesi olasılığı vardır.
Mavimsi arka plan
Düzgün bir şekilde renklendirilmiş bir arka plan kırmızı olacaktır. Mavi arka plan, renk atmasının yetersiz olduğunu gösterir.
referanslar
- Ryan KJ, Ray C. 2010. sherris. mikrobiyoloji Medical, 6. basım McGraw-Hill, New York, ABD
- Koneman E, Allen S, Janda W, Schreckenberger P, Winn W. (2004). Mikrobiyolojik tanı (5. basım). Arjantin, Editör Panamericana S.A..
- Forbes B, Sahm D, Weissfeld A. 2009. Bailey & Scott'un Mikrobiyolojik Tanısı. 12 ed. Arjantin. Panamericana S.A Editörden
- Casas-Rincón G. 1994. Genel Mikoloji. 2. Baskı, Universidad Central de Venezuela, Kütüphane baskıları. Venezuela, Caracas.
- "Gram boyası" Vikipedi, özgür ansiklopedi. 4 Ekim 2018, 23:40 UTC. 9 Aralık 2018, 17:11. Es.wikipedia.org sitesinden alınmıştır..
- González M, González N. 2011. Tıbbi Mikrobiyoloji El Kitabı. 2. Baskı, Venezuela: Medya ve Carabobo Üniversitesi Yayınları Müdürlüğü.
- López-José L, Hernández-Durán M, Colín-Castro C, Ortega-Peña S, Cerón-González G, Franco-Cendejas F. Mikrobiyoloji laboratuvarında temel boyama. Engellilik Araştırmaları. 2014; 3 (1): 10-18.


