Alüminyum sülfat (Al2 (SO4) 3) yapısı, kullanımı, çeşitleri, toksisite
alüminyum sülfat Al formülünün bir inorganik alüminyum tuzudur2(SO4)3, bu genellikle parlak kristallerle beyaz bir katı gibi görünür. Bileşiğin rengi, demir konsantrasyonundan ve diğer kirliliklerden etkilenecektir. İki ana alüminyum sülfat türü vardır: A ve B.
Alt resimde, beyaz hidratlanmış alüminyum sülfat kristalleri gösterilmektedir. Kristal örgü içindeki demir iyonlarının göstergesi olan kahverengi renklerin yokluğu belirtilebilir..

Alüminyum sülfat, suda çok çözünür bir tuzdur ve doğada, susuz formunda bulunması nadirdir. Genellikle oktadekahidrat alüminyum sülfat formunda hidratlanır [Al2(SO4)3.18H2O] veya heksadekahidrat [Al2(SO4)3.16H2O].
Aynı şekilde, potasyum ve amonyum ile çiftler olarak bilinen bileşikler oluşturabilir. Bu kısmen alüminyumun yanı sıra diğer iyonları tutmak için hidratlar içindeki suyun afinitesinden dolayı olabilir..
Alüminyum sülfat, suyun alüminyum hidroksit ve sülfürik asit içindeki etkisiyle ayrıştırılabilir. Bu özellik, toprak asitleştiricisi olarak kullanılmasına izin vermiştir..
Aynı zamanda, özellikle de tozu ile temasında toksik bir bileşiktir. Bununla birlikte, birkaç sanayide kullanımıyla gerçekleşen pıhtılaşma yöntemi ile suyun arıtılmasından, terapötik amaçlarla kullanılmasına kadar süren kullanım ve uygulamaların sonsuzluğuna sahiptir..
indeks
- 1 yapı
- 2 Ne için (kullanır)
- 2.1 Pıhtılaşma veya suyun topaklaşması
- 2.2 Bir mürekkep mordanı olarak ve kağıdın hazırlanmasında kullanın
- 2.3 Endüstriyel kullanımlar
- 2.4 Tıbbi ve terapötik kullanımlar
- 2.5 Diğer kullanımlar
- 3 Alüminyum sülfat üretimi
- 4 Çeşitleri
- 5 Toksisite
- 6 Kaynakça
yapı
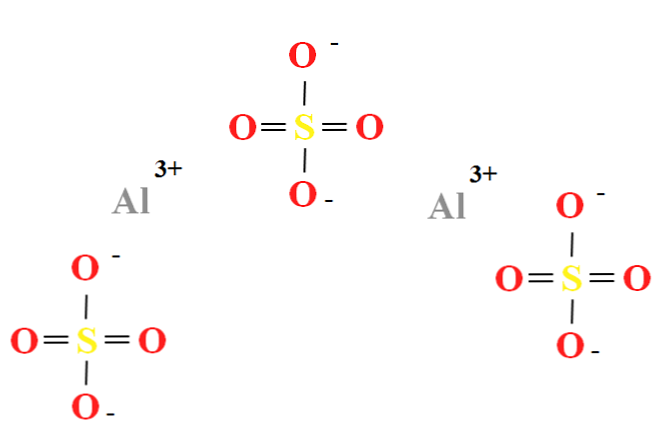
Alüminyum sülfat iki Al katyon oranına sahiptir3+ her üç anyon için SO42- (üstten görüntü), Al kimyasal formülü içinde doğrudan görülebilir.2(SO4)3.
Not Al3+ onlar grimsi42- sarı (kükürt atomu için) ve kırmızı (oksijen atomu için).
Gösterilen yapı Al'in susuz formuna tekabül eder2(SO4)3, çünkü hiçbir su molekülü iyonlarla etkileşime girmez. Bununla birlikte, hidratlarınızda, Al'ın pozitif merkezlerine su çekilebilir.3+, veya negatif SO tetrahedra tarafından42- hidrojen bağlarıyla (HOH-O-SO32-).
Al2(SO4)3∙ 18H2Veya, örneğin, katı yapısında 18 su molekülü içerir. Bazıları Al ile doğrudan temas halinde olabilir.3+ veya SO ile42-. Başka bir deyişle: alüminyum sülfat iç veya dış koordinasyon suyuna sahip olabilir..
Ayrıca, yapısı Fe gibi diğer katyonları barındırabilir3+, na+, K+, vb Ancak bunun için, daha fazla anyonların varlığı gereklidir.42-. Ne için? Metalik yabancı maddeler nedeniyle pozitif yüklerdeki artışı etkisiz hale getirmek için.
Alüminyum sülfat birçok yapıya sahip olabilir, ancak hidratları monoklinik kristal sistemi benimseme eğilimindedir..
Fiziksel ve kimyasal özellikler
görünüm
Parlak beyaz kristaller, granüller veya toz içeren bir katı madde gibi görünür..
Moleküler ağırlık
342.31 g / mol (susuz).
koku
Kokusuzdur
lezzet
Orta derecede sıkılaştırıcı tat.
Erime noktası
770º C susuz form (86.5º C oktadekahidratada form)
Suda çözünürlük
0 ° C'de 31.2 g / 100 ml; 36.4 g / 100 ml, 20 ° C'de ve 89 g / 100 ml, 100 ° C'de.
yoğunluk
2,67 - 2,71 g / cm3.
çözünürlük
Etil alkolde az çözünür.
Buhar basıncı
Temelde sıfır.
kararlılık
Havada kararlı.
ayrışma
Isıtıldığında, yaklaşık erime noktasında, özellikle zehirli bir gaz olan kükürt oksit yayarak ayrışabilir..
tahribat
Alüminyum sülfat çözeltileri alüminyumu aşındırır. Ayrıca bileşik, nemin varlığında metalleri paslandırabilir.
pKa
3,3 ila 3,6. Ve pH'ı,% 5'lik bir sulu çözelti içerisinde 2.9 veya daha fazladır.
Ne için (kullanır)
Suyun pıhtılaşması veya pıhtılaşması
-Su ile karıştırıldığında (içilebilir, servis veya atık), alüminyum sülfat çözeltideki bileşikler ve partiküller ile kompleksler oluşturan alüminyum hidroksitin oluşmasına neden olur; uzun zaman.
-Alüminyum sülfat ayrıca yüzme havuz suyunun temizliğinde de kullanılır ve kullanım için daha çekici hale getirilir..
-Alüminyum sülfat kullanımı ile bulanıklık ve renk olmadan su elde edilir, suyun temizlenmesini kolaylaştırarak pota kabiliyeti arttırılır. Maalesef, bu saflaştırma yöntemi su içinde hafifçe artan bir alüminyum konsantrasyonuna yol açabilir.
-Alüminyum deride, beyinde ve ciğerlerinde biriken ve ciddi hastalıklara neden olan çok toksik bir metaldir. Ayrıca, canlılarda hangi işlevi yerine getirdiği bilinmemektedir..
-Avrupa Birliği, su içinde izin verilen maksimum alüminyum limitinin 0,2 mg / l'yi geçmemesini gerektirir. Bu arada, ABD Çevre Koruma Ajansı, alüminyum ile maksimum su kirliliği sınırının 0,05-0,2 mg / l'yi geçmemesini gerektiriyor.
-Atık suyun arıtılması veya alüminyum sülfat ile kullanılması, bunların içindeki fosforun ortadan kaldırılmasını veya azaltılmasını sağlar..
Mürekkeplerin bir mordanı olarak ve kağıdın hazırlanmasında kullanın
-Boyanacak malzemeye sabitlemeye yardımcı olmak için boyalar veya mürekkepler için bir mordan olarak alüminyum sülfat kullanılmıştır. Sabitleme hareketi Al (OH) nedeniyledir.3, jelatinimsi kıvamı, boya maddelerinin tekstiller üzerine adsorpsiyonuna katkıda bulunur.
-MÖ 2000'den bu yana tarif edilen amaç için kullanılmış olmasına rağmen, sadece organik boyalar kolye gerektirir. Diğer taraftan, sentetik boyalar, mordanların işlevlerini yerine getirmelerini gerektirmez..
-Kâğıt imalatından uzaklaştırılmıştır, ancak yine de kağıt hamuru üretiminde kullanılmaktadır. Malzemeleri bağlamak, yükleri nötralize etmek ve reçine ayarlamak için kullanılan yabancı maddeleri uzaklaştırır..
Endüstriyel kullanımlar
-Beton yapımını hızlandırmak için inşaat sektöründe kullanılır. Ek olarak, binaların su yalıtımında kullanılır.
-Sabun ve yağ endüstrisinde, gliserin üretiminde kullanılır.
-Petrol endüstrisinde, işlem sırasında kullanılan sentetik katalizörlerin imalatında kullanılır..
-İlaç endüstrisinde ilaç ve kozmetik ürünlerinin hazırlanmasında büzücü olarak kullanılır..
-Karmin gibi boyaların üretilmesine müdahale eder. Bütadien stiren sentetik kauçuklarının imalatında da boya olarak kullanılır..
-Şeker imalat sanayinde şeker kamışı için pekmez arındırıcısı olarak kullanılır..
-Deodorant üretiminde kullanılır. Neden? Ter bezlerinin kanallarının daralmasına neden olduğu için ter birikimini sınırlandırır, böylece kokuya neden olan bakterilerin büyümesi için gerekli bir ortamdır..
-Deri tabaklamada kullanılır, kullanımı için gerekli işlemdir. Ek olarak, gübrelerin imalatında kullanılır..
-Boya, yapıştırıcı ve dolgu macunlarının yanı sıra mobilya temizliği ve bakım ürünlerinin hazırlanmasında katkı maddesi olarak kullanılır..
Tıbbi ve terapötik kullanımlar
-Alüminyum sülfat immünolojik bir adjuvandır. Bu nedenle, antijenleri, işlem yerlerinde serbest bırakıldıklarında, aşılanan antijenler için daha fazla antikor üretimi üretecek şekilde işleme fonksiyonunu yerine getirir..
-Freund adjuvanı ve BCG'nin yanı sıra, interlökinler gibi endojen olanlar dahil diğer adjuvanlar, immün etkinin yarıçapında bir artışa izin veren antijenler için spesifik değildir. Bu, birçok hastalığa karşı aşı geliştirilmesine olanak sağlamıştır..
-Alüminyum sülfatın pıhtılaştırıcı etkisi diğerlerinin yanı sıra arıtılmış sudaki sayısız virüsün ortadan kaldırılmasını sağlamıştır: Q beta, MS2, T4 ve Pl. Sonuçlar, suyun alüminyum sülfat ile arıtılmasının, bu tür virüslerin etkisizleşmesine neden olduğunu göstermektedir..
-Alüminyum sülfat, tıraş sırasında üretilen küçük yüzeysel yaraların veya sıyrıkların tedavisinde çubuk veya toz halinde kullanılır..
-Bazı kulak koşullarının tedavisinde kullanılan bir bileşik olan alüminyum asetatın yapımında kullanılır. Ayrıca, önemli bir başarı olmadan, ateş karıncası ısırıklarının sonuçlarını hafifletmek için kullanılmıştır..
-Aluminyum sülfat çözeltileri, salgılarının kontrolünü sağlayan ülserlerin lokal tedavisinde,% 5 ila% 10 konsantrasyonda kullanılır..
-Aliminyum sülfatın büzücü etkisi, cildin yüzeysel tabakalarına büzülür, proteinleri pıhtılaştırır ve yaraları iyileştirir.
Diğer kullanımlar
-Alüminyum sülfat, göletlerde, göllerde ve su akıntılarında alglerin aşırı büyümesinin kontrolüne yardımcı olur. Yumuşakçaların giderilmesinde, İspanyol sümüklü böceklerin yanı sıra.
-Bahçıvanlar bu bileşiği alkali toprakları asitleştirmek için uygular. Suyla temas halinde alüminyum sülfat alüminyum hidroksit içine ayrışır ve seyreltik sülfürik asit. Daha sonra, alüminyum hidroksit çökerek sülfürik asidi çözelti içinde bırakarak.
-Sülfürik asitten dolayı toprakların asitlendirilmesi, çiçekleri asidik toprak mevcudiyetinde maviye dönüşen Hydrangea adlı bir bitkinin varlığından dolayı çok yaratıcı bir şekilde görselleştirilmiştir; yani, duyarlıdırlar ve pH'daki değişikliklere cevap verirler..
-Alüminyum sülfat, yangına karşı mücadele ve kontrol için bir köpük üretiminde rol oynar. Nasıl? Sodyum bikarbonat ile reaksiyona girerek CO salınımını sağlar2. Bu gaz O erişimini engeller.2 malzemenin yanma yerine; ve sonuç olarak gelişmekte olan ateşkes.
Alüminyum sülfat üretimi
Alüminyum sülfat, boksit cevheri gibi alüminyumca zengin bir bileşiğin yüksek sıcaklıklarda sülfürik asitle reaksiyona sokulmasıyla sentezlenir. Aşağıdaki kimyasal denklem reaksiyonu temsil eder:
için2Ey3 + 'H2GB4 -> Al2(SO4)3 + 3 H2Ey
Alüminyum sülfat, aşağıdaki reaksiyona göre, alüminyum hidroksit ve sülfürik asit arasındaki nötrleştirme reaksiyonu ile de oluşturulabilir:
2 Al (OH)3 + 3 H2GB4 + 12 H2O -> Al2(SO4)3.18H2Ey
Sülfürik asit, amonyum sülfat oluşturmak için alüminyum ile reaksiyona girer ve gaz halinde hidrojen moleküllerinin salınımını sağlar. Reaksiyon aşağıdaki gibi şematikleştirilmiştir:
2 Al + 3 H2GB4 -> Al2(SO4)3 + 3 H2
tip
Alüminyum sülfat iki tipte sınıflandırılır: tip A ve tip B. Alüminyum sülfat tip A'da, katılar beyazdır ve% 0.5'den az demir konsantrasyonuna sahiptir..
B tipi alüminyum sülfatta katılar kahverengidir ve% 1.5'den az demir konsantrasyonuna sahiptir..
Sınıflandırılmasında farklı kriterleri olan alüminyum sülfat üreten endüstriler var. Bu nedenle, bir endüstri, A tipi alüminyum sülfatın hazırlandığını bildirir ve ferrik oksit olarak maksimum% 0.1 demir konsantrasyonu. B tipi için ise maksimum% 0.35 demir konsantrasyonunu gösterir..
toksisite
-Alüminyum sülfat, tozuyla temas ederek toksik etki gösteren, böylece cildin tahriş olmasına ve temasın sık olduğu durumlarda bir dermatite neden olan bir bileşiktir..
-Gözlerde kalıcı yaralanmalara neden olsa bile güçlü bir tahrişe neden olur.
-Soluma burun ve boğazın tahriş olmasına neden olur, bu da öksürük ve döküntülere neden olabilir.
-Alımı gastrik tahrişe, mide bulantısına ve kusmaya neden olur.
-Doğrudan alüminyum sülfat nedeniyle olmasalar da, dolaylı olarak kullanımlarından dolayı toksik etkileri vardır. Suyun arıtılmasında alüminyum sülfat kullanımının neden olduğu alüminyumun bazı toksik etkileri söz konusudur..
-Saflaştırılmış suda hazırlanan tuzlar kullanılarak, kronik olarak diyaliz edilen hastalar, alüminyum sülfat kullanılarak, çok ciddi sağlık bozuklukları yaşarlar. Bu bozukluklar arasında anemi, diyalizle demans ve kemik hastalıklarında artış var..
referanslar
- Vikipedi. (2018). Alüminyum sülfat Alındığı kaynak: en.wikipedia.org
- Aris Endüstri A ve B tipi alüminyum sülfat çözeltisi
- Christopher Boyd (9 Haziran 2014). Aluminyum Sülfatın Endüstriyel Kullanımı. Alındığı yer: chemservice.com
- Pubchem. (2018). Alüminyum Sülfat Susuz. Alındığı kaynak: pubchem.ncbi.nlm.nih.gov
- Andesia Kimyasalları (20 Ağustos 2009). Alüminyum sülfat güvenlik levhası. [PDF]. Alındığı kaynak: andesia.com
- Kimyasal Kitap (2017). Alüminyum Sülfat Alındığı kaynak: chemicalbook.com


