Alüminyum Klorür (AlCl3) kimyasal yapısı, özellikleri, kullanım alanları
alüminyum klorür veya alüminyum triklorür (AlCl3) alüminyum ve klorin oluşturduğu ikili bir tuzdur. Bazen sarı bir toz halinde görünür, çünkü demir (III) klorür varlığından dolayı safsızlıklar sunar..
Elementleri birleştirerek elde edilir. Son enerji seviyesinde üç elektrona sahip olan alüminyum (aile IIIA), metalik karakterinden dolayı onları üretme eğilimindedir. Son enerji seviyesindeki yedi elektronlu Klor (VIIA ailesi), octetini tamamlamaları için onları kazanma eğilimindedir..
Metal ve metal olmayanlar arasında bir birliktelik olmasına rağmen, alüminyum triklorürde alüminyum ile klor arasında oluşan bağın kovalent olduğu düşünülmektedir..
İki çeşit alüminyum klorür vardır:
- Susuz alüminyum klorür. AlCl3.
- Alüminyum klorür heksahidrat. AlCl3. 6H2O. Bu bileşik katı veya çözelti halinde bulunabilir.
indeks
- 1 Kimyasal yapı
- 2 Özellikler
- 2.1 Fiziksel
- 2.2 Kimyasal
- 3 Kullanım
- 4 Riskler: olası etkiler
- 5 Tavsiye
- 6 Kaynakça
Kimyasal yapısı
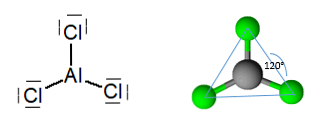
Susuz alüminyum triklorür, bir atomik hibridizasyon sp'ye karşılık gelen 120 ° 'lik bir açı ile düzlemsel bir trigonal geometriye sahip bir moleküldür.2.
Bununla birlikte, molekül şeklinde düzenlenir dimerleri, içinde bir klorin atomu, bağlar oluşturmak için bir çift elektron bağışlar. Bunlar koordine kovalent bağlar olarak bilinir..
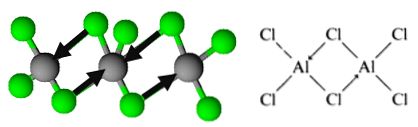
Bu, alüminyum triklorür dimerlerinin organizasyonunun nasıl çıkarılacağıdır..
Bu organizasyon, bileşiğin, dimerik katman ağları oluşturmasını sağlar. Katı alüminyum triklorür üzerine su dökülürken iyonik bileşiklerden beklendiği gibi ayrışmazlar, ancak kuvvetli hidrolize uğrarlar.
Aksine, seyreltilmiş sulu çözeltide koordine edilmiş iyonlar [Al (H)2O)6]+3 ve klorür. Bu yapılar diboraninkine çok benzer.
Bu şekilde Al formülüne sahip olursunuz.2Cı6
Bu bileşikteki bağları oluşturan atomların elektronegatiflikteki fark ölçülürse, aşağıdakiler gözlemlenebilir:
Aluminyum Al için elektronegatiflik değeri 1,61 C, klorin değeri 3,16 C'dir. Elektronegativite farkı 1,55 C'dir..
Bağlanma teorisinin kurallarına göre, bir bileşiğin iyonik olması için, 1.7 C'ye eşit veya daha büyük bir değerin bağını oluşturan atomların elektronegatifliği arasında bir fark olması gerekir..
Al-Cl bağı durumunda, elektronegatiflikteki fark, alüminyum triklorüre kovalent bir bağlanma düzeneği veren 1.55 C'dir. Bu küçük değer, molekül tarafından sunulan koordineli kovalent bağlara bağlanabilir..
özellikleri
fiziksel
görünüm: beyaz katı, bazen de ferrik klorürün neden olduğu safsızlıklar nedeniyle sarı
yoğunluk: 2.48 g / mL
Molar kütle: 133.34 g / mol
yüceltme: 178 ° C'de süblime olur, bu nedenle erime ve kaynama noktaları çok düşüktür.
sürme: zayıf elektrik iletiyor.
çözünürlük: Suda çözünür değildir, çünkü Lewis asididir. Benzen, karbon tetraklorür ve kloroform gibi organik çözücülerde çözünür.
kimyasal
Suda, alüminyum triklorür, HCI ve hidronyum iyonu ve alüminyum hidroksit oluşturan hidrolize edilir:
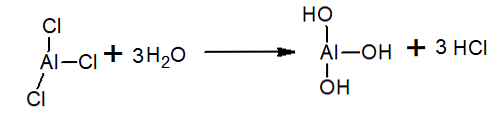
Friedel-Crafts reaksiyonlarında katalizör olarak kullanılır (reaksiyon sonunda geri kazanılabilen madde, çünkü sadece reaksiyonu hızlandırmak, yavaşlatmak veya başlatmak için vardır).
Aşındırıcı bir maddedir.
Ayrışmasında suyla şiddetli reaksiyona girdiğinde alüminyum oksit ve hidrojen klorid gibi tehlikeli gazlar çıkarır..
uygulamaları
- terlemeyi önleyici.
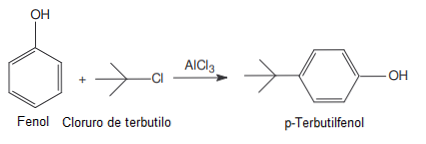
- Friedel-Crafts'in asilasyonu ve alkilasyonunda katalizör.
Riskler: olası etkiler
- Aşındırıcı bir maddedir, ciltte yanıklara ve ciddi göz hasarına neden olur..
- Su ile şiddetli reaksiyon verir.
- Çevre için tehlikelidir.
- Sudaki organizmalar için çok toksik.
tavsiyeler
Gerekli güvenlik önlemleri alınmadan ürüne maruz kalmaktan kaçının. Kullanmalı, koruyucu gözlük, eldiven, uygun kıyafet, kapalı ayakkabı.
Solunması halinde. Tozun solunması, maddenin aşındırıcı yapısından dolayı solunum sistemini tahriş edebilir. Belirtileri boğaz ağrısı, öksürük ve nefes darlığıdır. Akciğer ödemi belirtileri geç olabilir ve ciddi vakalar ölümcül olabilir. Kurbanı kirletici olmayan havadar bir yere götürün. Gerekirse suni solunum sağlayın. Nefes almakta zorluk çekiyorsanız, oksijen verin. Doktoru ara.
Cilt teması durumunda. AlCl3 Aşındırıcıdır. Tahrişe neden olabilir veya kızarıklık ve acı ile yanmalara neden olabilir. En az 20 dakika boyunca bol su ile yıkadıktan sonra yıkayınız. Nötrleştirmeyin veya su dışındaki maddeleri eklemeyin. Kirlenmiş giysileri çıkarın ve yeniden kullanmadan önce yıkayın. Yaralanma durumunda derhal doktora danışın..
Gözlerle teması üzerine. AlCl3 Aşındırıcıdır. Yoğun ağrı, bulanık görme ve doku hasarına neden olur. Gözleri derhal en az 20 dakika suyla yıkayın ve göz kapağının tüm göz ve dokularının temizlendiğinden emin olmak için göz kapaklarını açık tutun. Maksimum verimlilik elde etmek için gözleri birkaç saniye içinde yıkamak çok önemlidir. Kontakt lensleriniz varsa, ilk 5 dakika sonra onları çıkarın ve sonra gözlerinizi durulamaya devam edin. Doktora danışın. Kornea, konjonktiva veya gözün diğer kısımlarında ciddi hasara neden olabilir.
Yutulması halinde. AlCl3 Aşındırıcıdır. Yanma ağızda ve yemek borusunda ağrıya ve mukoza zarının yanmasına neden olabilir. Karın ağrısı, bulantı, kusma ve ishal ile gastrointestinal rahatsızlık yaratabilir. Kusmaya karar vermeyin. Ağzınızı çalkalayın ve içmesi için su verin. Bilinci yerinde olmayan kişilere asla ağızdan bir şey vermeyin. Doktoru ara. Kusma kendiliğinden meydana gelirse, aspirasyon riskini azaltmak için mağduru kendi tarafına koyun..
Mevcut cilt hastalıkları veya göz problemleri veya solunum fonksiyonlarının bozulması olan kişiler maddenin etkisine daha duyarlı olabilirler
AlCl bileşiğinin paketlenmesi ve depolanması3 Havalandırılmış, temiz ve kuru yerlerde yapılmalıdır..
referanslar
- Kimya kitabı, (2017), Aluminyum klorür. Chemicalbook.com adresinden kurtarıldı
- cosmos çevrimiçi, cosmos.com.mx
- Sharpe, A.G., (1993), Organik Kimya, İspanya, Editoryal Reverté, S.A..
- F., (2017), AlCl Alüminyum Klorür3, Insignia. -Den alınanblog.elinsignia.com.
- TriHealth, (2018), Alüminyum Triklorür, son güncelleme, 4 Mart 2018, Trihealth.adam.com adresinden alınmıştır..
- RxWiki, (s.f), Aliminyum Klorür, Alınan, rxwiki.com.


