Susuz özellikler, nasıl oluştukları, adlandırılması, uygulamaları
anhidridler Suyun serbest bırakılması yoluyla iki molekülün birleşmesinden kaynaklanan kimyasal bileşiklerdir. Böylece, başlangıçtaki maddelerin dehidrasyonu olarak görülebilir; tam olarak doğru olmasa da.
Organik ve inorganik kimyada bunlardan söz edilir ve her iki dalda da anlayışı kayda değer ölçüde farklılık gösterir. Örneğin inorganik kimyada bazik ve asitli oksitler, bunların ikincisi oluşturmak için suyla reaksiyona girdiklerinden, sırasıyla hidroksitlerinin ve asitlerinin anhidritleri olarak kabul edilir..

Burada “susuz” ve “susuz” terimleri arasında karışıklık ortaya çıkabilir. Genellikle susuz, kimyasal yapısında değişiklik olmadan susuz kalmış bir bileşiği ifade eder (reaksiyon yok); bir anhidrit ile moleküler yapıya yansıyan kimyasal bir değişim söz konusuysa.
Hidroksit ve asitler karşılık gelen oksitlerle (veya anhidritlerle) karşılaştırılırsa, bir reaksiyon olduğu görülecektir. Buna karşılık, bazı oksitler veya tuzlar hidratlanabilir, su kaybedebilir ve aynı bileşikler kalabilir; ama susuz, susuz.
Diğer taraftan organik kimyada, anhidrit ile kastedilen ilk tanımdır. Örneğin, en bilinen anhidritlerden biri karboksilik asitlerin türevleridir (üstten görüntü). Bunlar, bir oksijen atomu vasıtasıyla iki asil grubunun (-RCO) birleşmesinden oluşur..
Genel yapısında R belirtilmiştir1 bir asil grubu için ve R2 ikinci asil grubu için. Çünkü R1 ve R2 farklıdırlar, farklı karboksilik asitlerden gelirler ve daha sonra asimetrik bir asit anhidrittir. Her iki R ikame edicisi de (aromatik olsun olmasın) aynı olduğunda, simetrik bir asit anhidrit durumundan söz ediyoruz..
Anhidrürü oluşturmak için iki karboksilik asit bağlanması sırasında, su, diğer bileşiklerin yanı sıra oluşturulabilir veya olmayabilir. Her şey söz konusu asitlerin yapısına bağlı olacak.
indeks
- 1 Anhidritlerin Özellikleri
- 1.1 Kimyasal reaksiyonlar
- 2 Anhidritler nasıl oluşur??
- 2.1 Döngüsel anhidritler
- 3 İsimlendirme
- 4 uygulama
- 4.1 Organik anhidritler
- 5 Örnekler
- 5.1 Süksinik anhidrit
- 5.2 Glutarik anhidrit
- 6 Kaynakça
Anhidritlerin Özellikleri
Anhidritlerin özellikleri, neyi kastettiğinize bağlı olacaktır. Neredeyse hepsinin ortak bir özelliği suyla reaksiyona girmeleridir. Bununla birlikte, inorganik olarak adlandırılan bazik anhidritler için, aslında birçoğu suda bile çözünmez (MgO), bu nedenle bu açıklama karboksilik asitlerin anhidritlerine odaklanacaktır..
Erime ve kaynama noktaları, (RCO) için moleküler yapı ve moleküller arası etkileşimler üzerine düşer.2Veya bu organik bileşiklerin genel kimyasal formülüdür..
Eğer moleküler kütle (RCO) ise2Veya düşük, muhtemelen oda sıcaklığında ve basınçta renksiz bir sıvıdır. Örneğin, asetik anhidrit (veya etanoik anhidrit), (CH3CO)2Ya da, bir sıvıdır ve daha büyük endüstriyel öneme sahip olan, üretimi çok geniştir..
Asetik anhidrid ve su arasındaki reaksiyon, aşağıdaki kimyasal denklem ile temsil edilir:
(CH3CO)2O + H2O => 2CH3COOH
Su molekülü eklendiğinde, iki asetik asit molekülünün serbest kaldığına dikkat edin. Bununla birlikte, ters reaksiyon asetik asit için gerçekleşemez:
2CH3COOH => (CH3CO)2O + H2O (Olmaz)
Başka bir sentetik rotaya başvurmak gereklidir. Dikarboksilik asitler ise ısıtılarak; ancak bir sonraki bölümde açıklanacaktır.
Kimyasal reaksiyonlar
hidroliz
Anhidritlerin en basit reaksiyonlarından biri, asetik anhidrit için gösterilmiş olan hidrolizleridir. Bu örneğe ek olarak, sülfürik asit anhidritine sahibiz:
'H2S2Ey7 + 'H2Ey <=> 2H2GB4
Burada bir inorganik asit anhidrürünüz var. H için not edin2S2Ey7 (ayrıca disülfürik asit de denir), reaksiyonun kendisi geri dönüşümlüdür, bu nedenle H ısıtılır2GB4 Konsantre, anhidritinin oluşumuyla sonuçlanır. Öte yandan, H'nin seyreltilmiş bir çözeltisi ise,2GB4, SO serbest bırakıldı3, sülfürik anhidrit.
esterleştirme
Asit anhidritler, bir ester ve bir karboksilik asit verecek şekilde ortamdaki piridin ile alkollerle reaksiyona girer. Örneğin, asetik anhidrit ve etanol arasındaki reaksiyon göz önünde bulundurulur:
(CH3CO)2O + CH3CH2OH => CH3CO2CH2CH3 + CH3COOH
Böylece etil ester etanoat, CH oluşturan3CO2CH2CH3, ve etanoik asit (asetik asit).
Pratik olarak, olan, hidroksil grubunun hidrojeninin bir asil grubu ile ikame edilmesidir:
R,1-OH => R1-OCOR2
(CH durumunda)3CO)2Veya, asil grubunuz -COCH'dir.3. Bu nedenle, OH grubunun asilasyon yaşadığı söylenir. Bununla birlikte, asilasyon ve esterleştirme, birbiriyle değiştirilebilir kavramlar değildir; Asilasyon doğrudan Friedel-Crafts asilasyonu olarak bilinen aromatik bir halkada gerçekleşebilir..
Böylece asit anhidritlerin varlığında alkoller bir asilasyon ile esterleştirilir..
Öte yandan, iki asil grubundan sadece biri alkolle reaksiyona girmekte, diğeri hidrojen ile kalmaktadır; bunun için (CH3CO)2Ya da etanoik asit..
amidasyon
Asit anhidritler, amidleri vermek üzere amonyakla veya aminlerle (birincil ve ikincil) reaksiyona girer. Reaksiyon, tarif edilen esterleşmeye çok benzer, ancak ROH, bir amin ile değiştirilir; örneğin, ikincil bir amin, R2NH.
Yine, (CH arasındaki reaksiyon)3CO)2O ve dietilamin, Et2NH:
(CH3CO)2O + 2Et2NH => CH3CoNet2 + CH3COO-+NH2ve2
Ve dietilasetamid, CH oluşur3CoNet2, ve bir karboksilik amonyum tuzu, CH3COO-+NH2ve2.
Denklem anlamak biraz zor gibi görünse de, -COCH grubunun nasıl olduğunu gözlemlemek yeterli3 Et'in H'sinin yerini alır2Amiti oluşturmak için NH:
ve2NH => Et2NCOCH3
Bir amidasyondan daha fazla, reaksiyon hala bir asilasyondur. Her şey bu kelimeyle özetlenir; bu sefer, amin alkolü değil asilasyonu çekiyor.
Anhidritler nasıl oluşur??
İnorganik anhidritler, elementin oksijen ile reaksiyona sokulması suretiyle oluşturulur. Böylece, element metalik ise, bir baz metal oksit veya anhidrit oluşur; ve metalik değilse, metalik olmayan bir oksit veya asit anhidrit oluşur.
Organik anhidritler için reaksiyon farklıdır. İki karboksilik asit, suyu serbest bırakmak ve asit anhidrid oluşturmak için doğrudan bağlanamaz; Henüz belirtilmeyen bir bileşiğin katılımı gereklidir: asil klorür, RCOCl.
Karboksilik asit, asil klorür ile reaksiyona girerek ilgili anhidrit ve hidrojen klorürü üretir:
R,1COCl + R2COOH => (R1CO) O (COR2) + HCI
CH3COCI + CH3COOH => (CH3CO)2O + HCI
Bir CH3 asetil grubundan gelir, CH3CO- ve diğeri asetik asit içinde zaten var. Belirli bir asil klorürün yanı sıra karboksilik asidin seçimi, simetrik veya asimetrik bir asit anhidritin sentezine yol açabilir.
Siklik anhidritler
Bir asil klorür gerektiren diğer karboksilik asitlerin aksine, dikarboksilik asitler karşılık gelen anhidritlerinde yoğunlaştırılabilir. Bunun için, H salınımını teşvik etmek için onları ısıtmak gerekir.2O. Örneğin, ftalik asitten ftalik anhidrit oluşumu gösterilmiştir.

Beşgen halkanın nasıl tamamlandığına ve her iki gruba da bağlanan oksijenin C = O'nun bir parçası olduğuna dikkat edin; Bu bir siklik anhidrittir. Ayrıca, ftalik anhidritin, her iki R'den beri, simetrik bir anhidrit olduğu görülebilir.1 R olarak2 Onlar aynıdır: aromatik bir halka.
Tüm dikarboksilik asitler anhidritlerini oluşturamazlar, çünkü COOH grupları geniş ölçüde ayrıldığında, daha büyük ve daha büyük halkaları tamamlamak zorunda kalırlar. Oluşabilecek en büyük halka, reaksiyonun gerçekleşmediğinden daha büyük olan altıgen bir halkadır.
terminoloji
Anhidritler nasıl adlandırılır? Oksitlerle ilgili inorganikleri bir kenara bırakmak, şimdiye kadar açıklanan organik anhidritlerin adları, R'nin kimliğine bağlıdır.1 ve R2; yani asil gruplarından.
Eğer iki R aynı ise, 'asit' kelimesini 'anhidrit' yerine karboksilik asit adına yazmanız yeterlidir. Ve eğer aksine, iki R farklıysa, alfabetik sıraya göre adlandırılırlar. Bu nedenle, ne diyeceğini bilmek için, öncelikle simetrik mi yoksa asimetrik bir asit anhidrit mi olduğunu görmek gerekir..
(CH3CO)2Ya da simetriktir, çünkü R1= R2 = CH3. Asetik veya etanoik asidin türevi, bu nedenle adı önceki açıklamaları takip eder: asetik anhidrit veya etanoik. Aynı şey, daha önce bahsedilen ftalik anhidrit için de geçerlidir..
Diyelim ki aşağıdaki anhidrit var:
CH3CO (O) COCH2CH2CH2CH2CH2CH3
Soldaki asetil grubu, asetik asitten, sağdaki ise heptanoik asitten gelir. Bu anhidriti adlandırmak için R gruplarınızı alfabetik sıraya göre adlandırmalısınız. Yani, adı: heptanoik asetik anhidrit.
uygulamaları
İnorganik anhidritler, malzemelerin, seramiklerin, katalizörlerin, çimentoların, elektrotların, gübrelerin vb. Sentezlenmesi ve formülasyonundan, binlerce demir ve alüminyum minerali ve dioksit ile yer kabuğunun kaplanmasına kadar çok sayıda uygulamaya sahiptir. canlı organizmalar tarafından tüketilen karbon.
İnorganik sentezde kullanılan birçok bileşiğin türetildiği nokta olan çıkış kaynağını temsil ederler. En önemli anhidritlerden biri karbondioksit, CO'dur.2. Su ile birlikte fotosentez için esastır. Ve endüstriyel düzeyde, SO3 sanık ondan sülfürik asit aldığı için çok önemlidir.
Belki de, daha fazla uygulama içeren ve (yaşam olduğu sürece) sahip olan anhidrit fosforik asitten biridir: daha iyi ATP olarak bilinen adenosin trifosfat, DNA'da bulunur ve metabolizmanın "enerjik para birimi".
Organik anhidritler
Asit anhidritler, bir asilasyonla, bir alkole, bir esteri meydana getirmeye, bir amine, bir amide veya bir aromatik halkaya neden olacak şekilde reaksiyona girer..
Bu bileşiklerin her birinin milyonları ve bir anhidrit hazırlamak için yüzbinlerce karboksilik asit seçeneği vardır; bu nedenle, sentetik olanaklar büyük ölçüde büyür.
Dolayısıyla, ana uygulamalardan biri, bir asil grubunu, bir bileşiğe bir asil grubunu dahil etmek, yapısının atomlarından veya gruplarından birini ikame etmek.
Her bir anhidrit ayrı ayrı kendi uygulamalarına sahiptir, fakat genel olarak hepsi benzer şekilde tepki verir. Bu nedenle, bu tip bileşikler, polimer yapılarını değiştirmek, yeni polimerler oluşturmak; yani, kopolimerler, reçineler, kaplamalar vs..
Örneğin, asetik anhidrid, tüm OH selüloz gruplarını asetillemek için kullanılır (alt görüntü). Bununla OH'nin her H'si bir asetil grubu olan COCH ile değiştirilir.3.
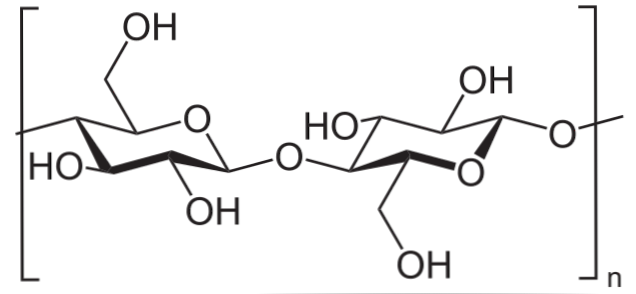
Bu şekilde selüloz asetat polimeri elde edilir. Aynı reaksiyon, NH grupları olan diğer polimer yapılar ile çizilebilir.2, ayrıca asilasyona duyarlı.
Bu asilasyon reaksiyonları, aspirin (asit gibi) ilaçların sentezi için de yararlıdır. asetilsalisilik).
Örnekler
Diğer bazı organik anhidrit örneklerinin bitmiş olduğu gösterilmiştir. Bunlardan bahsedilmemesine rağmen, oksijen atomları yerine kükürt, kükürt ve hatta fosfor anhidritleri verilebilir..
-C6'H5CO (O) COC6'H5: benzoik anhidrit. C grubu6'H5 bir benzen halkasını temsil eder. Hidrolizi iki benzoik asit üretir.
-HCO (0) COH: formik anhidrit. Hidrolizi iki formik asit üretir.
- C6'H5CO (O) COCH2CH3: benzoik propanoik anhidrit. Hidrolizi benzoik ve propanoik asitler üretir.
-C6'H11CO (O) COC6'H11: sikloheksankarboksilik anhidrit. Aromatik halkaların aksine, bunlar çift bağlar olmadan doyurulur.
-CH3CH2CH2CO (O) COCH2CH3: bütanoik propanoik anhidrit.
Süksinik anhidrit

Burada süksinik asitten bir dikarboksilik asitten türetilmiş başka bir siklik var. Üç oksijen atomunun bu tür bir bileşiğin kimyasal yapısına nasıl ihanet ettiğini görün.
Maleik anhidrit, süksinik anhidride çok benzerdir; fark, pentagonun tabanını oluşturan karbonlar arasında çift bir bağ bulunmasıdır..
Glutarik anhidrit
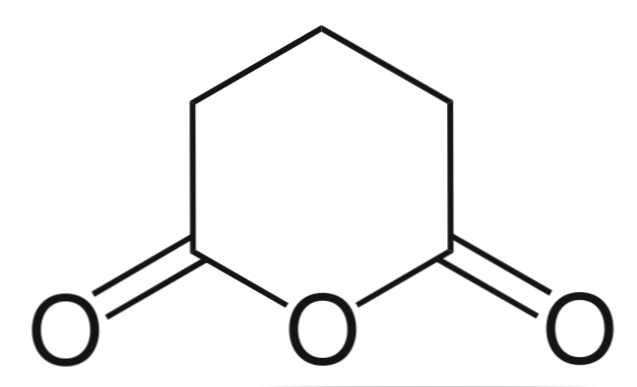
Ve son olarak, glutarik asidin anhidriti gösterilir. Bu yapısal olarak altıgen bir halkadan oluşan diğerlerinden ayırt edilir. Yine, üç oksijen atomu yapıda öne çıkıyor.
Daha karmaşık olan diğer anhidritler, birbirine çok yakın olan üç oksijen atomu tarafından her zaman kanıtlanabilir..
referanslar
- Ansiklopedi Britannica Editörleri. (2019). Anhidrit. Encryclopaedia Britannica. Alınan: britannica.com
- Helmenstine, Anne Marie, Ph.D. (8 Ocak 2019). Kimyada Asit Anhidrit Tanımı. Alınan adres: thoughtco.com
- Kimya LibreTexts. (N.D.). Anhidratlar. Şu kaynaktan alındı: chem.libretexts.org
- Graham Solomons T.W., Craig B. Fryhle. (2011). Organik Kimya Aminler. (10inci baskı.). Wiley Plus.
- Carey F. (2008). Organik Kimya (Altıncı baskı). Mc Graw Hill.
- Whitten, Davis, Peck ve Stanley. (2008). Kimya. (8. basım). CENGAGE Öğrenme.
- Morrison ve Boyd. (1987). Organik kimya (Beşinci baskı). Addison-Wesley Iberoamericana.
- Vikipedi. (2019). Organik asit anhidrit. Alınan: en.wikipedia.org


