Etil eter özellikleri, yapısı, elde edilmesi, kullanımı
etil eter, dietil eter olarak da bilinir, kimyasal formülü C olan organik bir bileşiktir4'H10O. Renksiz ve uçucu bir sıvı olması ile karakterizedir ve bu nedenle şişeleri mümkün olduğu kadar hava geçirmez şekilde kapatılmalıdır..
Bu eter dialkil eterlerin bir üyesi olarak sınıflandırılır; yani, R ve R 'farklı karbon segmentlerini temsil ettiği ROR' formülüne sahiptir. Ve onun orta adını tarif ettiği gibi, dietil eter, oksijen atomuna bağlanan iki radikal-etildir..

Başlangıçta etil eter, 1846'da William Thomas Green Morton tarafından tanıtılan genel bir anestezik olarak kullanıldı. Ancak, yanıcılığı nedeniyle, kullanımı daha az tehlikeli anesteziklerle değiştirilerek reddedildi..
Bu bileşik ayrıca, hastaların kardiyovasküler durumunun değerlendirilmesi sırasında, kan dolaşımını tahmin etmek için de kullanılmıştır..
Vücut içinde dietil eter karbondioksit ve metabolitlere dönüştürülebilir; Sonuncusu idrarla atılır. Bununla birlikte, uygulanan eterin çoğu, herhangi bir değişiklik yapmadan, akciğerlerde ekshale edilir.
Diğer taraftan, sabunlar, yağlar, parfümler, alkaloitler ve diş etleri için çözücü olarak kullanılır..
indeks
- 1 Etil eterin yapısı
- 1.1 Moleküller arası kuvvetler
- 2 Fiziksel ve kimyasal özellikler
- 2.1 Diğer isimler
- 2.2 Moleküler formül
- 2.3 Moleküler ağırlık
- 2.4 Fiziksel görünüm
- 2.5 Koku
- 2.6 Tat
- 2.7 Kaynama noktası
- 2.8 Erime noktası
- 2.9 Parlama noktası
- 2.10 Suda çözünürlük
- 2.11 Diğer sıvılarda çözünürlük
- 2.12 Yoğunluk
- 2.13 Buhar yoğunluğu
- 2.14 Buhar basıncı
- 2.15 Kararlılık
- 2.16 Otomatik ateşleme
- 2.17 Ayrıştırma
- 2.18 Viskozite
- 2.19 Yanma ısısı
- 2.20 Buharlaşma ısısı
- 2.21 Yüzey gerilimi
- 2.22 İyonlaşma potansiyeli
- 2.23 Koku eşiği
- 2.24 Kırılma indisi
- 3 Edinme
- 3.1 Etil alkolden
- 3.2 Etilen'den
- 4 Toksisite
- 5 kullanır
- 5.1 Organik çözücü
- 5.2 Genel anestezi
- 5.3 Eterin ruhu
- 5.4 Kan dolaşımını değerlendirme
- 5.5 Öğretim laboratuvarları
- 6 Kaynakça
Etil eterin yapısı
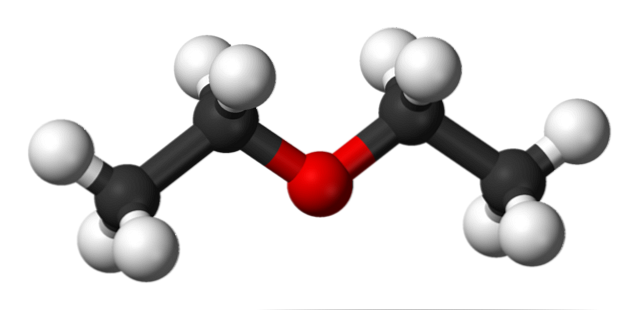
Yukarıdaki resimde, etil eter moleküler yapısına sahip bir küre modeli ve çubuk gösterimi var..
Görülebileceği gibi, oksijen atomuna karşılık gelen kırmızı küre, her iki tarafa da bağlı iki etil grubuna sahiptir. Tüm bağlantılar eksenlerin etrafında basit, esnek ve serbestçe dönebilir σ.
Bu rotasyonlar, uyumlu olanlar olarak bilinen stereoizomerleri oluşturur; izomerlerden daha fazla, alternatif mekansal devletlerdir. Görüntünün yapısı tam olarak, bütün atom gruplarının (birbirinden ayrılmış) şaşırtıldığı anti-konformere karşılık gelir..
Diğer üretici ne olabilir? Tutulmuştur, ve görüntünüz mevcut olmasa da, sadece U şeklinde görünmesini sağlayın U'nun üst uçlarında metil grupları yer alacak, -CH3, sterik itmeler yaşayacak (uzayda çarpışacaklardı).
Bu nedenle, CH molekülünün olması bekleniyor3CH2OCH2CH3 çoğu zaman anti-konformasyonu benimsemek.
Moleküller arası kuvvetler
Hangi moleküller arası kuvvetler gereği etil eter molekülleri sıvı fazda yönetilir? Dipol momentleri (1.5D), elektronik yoğunlukta (δ +) yeterince eksik bir bölgeye sahip olmadığından, esas olarak dispersiyon kuvvetleri sayesinde sıvıda tutulurlar.
Bunun nedeni, etil gruplarının hiçbir karbon atomunun, oksijen atomuna çok fazla elektron yoğunluğu vermemesidir. Yukarıdaki, eldeki eter eterin elektrostatik potansiyelinin haritası ile açıktır (alt görüntü). Mavi bir bölgenin bulunmadığına dikkat edin..
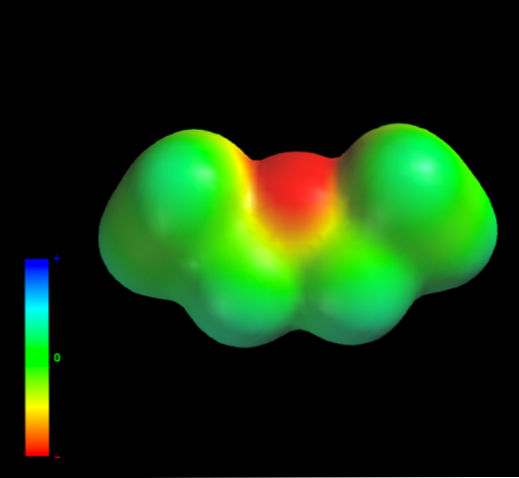
Oksijen, yine hidrojen bağları oluşturamaz, çünkü moleküler yapı içinde mevcut O-H bağları yoktur. Dolayısıyla, anlık dipoller ve dağılma kuvvetlerini destekleyen moleküler kütleleridir..
Buna rağmen, suda oldukça çözünür. Neden? Çünkü daha yüksek elektron yoğunluğuna sahip olan oksijen atomu bir su molekülünden hidrojen bağlarını kabul edebilir:
(CH3CH2)2Eyδ- - δ+'H-OH,
Bu etkileşimler, 100mL suda çözülen 6.04g eterden sorumludur..
Fiziksel ve kimyasal özellikler
Diğer isimler
-Dietil eter
-ethoxyethane
-Etil oksit
Moleküler formül
C4'H10O veya (C2'H5)2Ey.
Moleküler ağırlık
74.14 g / mol.
Fiziksel görünüm
Renksiz sıvı.
koku
Tatlı ve baharatlı.
lezzet
Yanan ve tatlı.
Kaynama noktası
94,3 ºF (34,6 ºC) ila 760 mmHg.
Erime noktası
-177.3 ºF (-116.3 ªC). Kararlı kristaller.
Ateşleme noktası
-49ºF (kapalı konteyner).
Suda çözünürlük
25 ° C'de 6.04 g / 100 mL.
Diğer sıvılarda çözünürlük
Kısa zincirli alifatik alkoller, benzen, kloroform, petrol eteri, yağ çözücü, birçok yağ ve konsantre hidroklorik asit ile karışabilir.
Asetonda çözünür ve etanolde çok çözünür. Aynı zamanda nafta, benzen ve yağlarda çözünür.
yoğunluk
68 ªF'de (20 ºC) 0.714 mg / mL.
Buhar yoğunluğu
2,55 (yoğunluk 1 ile alınan hava ile ilgili olarak).
Buhar basıncı
682F'de 442 mmHg. 25 ° C'de 538 mmHg 20 ºC'de 58.6 kPa.
kararlılık
Peroksit oluşumuyla hava, nem ve ışığın etkisiyle yavaşça oksitlenir..
Peroksitlerin oluşumu, açılmış ve altı aydan fazla bir süre depoda kalan eter kaplarında oluşabilir. Peroksitler sürtünme, darbe veya ısınma ile patlayabilir.
Şunlarla temastan kaçının: çinko, halojenler, metalik olmayan oksihalidler, güçlü oksitleyici ajanlar, kromil klorür, tementin yağları, nitratlar ve metal klorürler.
Otomatik ateşleme
356ºF (180ºC).
ayrışma
Isınırken ayrışır, keskin bir ses yayar ve tahriş edici duman çıkarır..
viskozite
20 ° C'de 0.2448 cPoise.
Yanma ısısı
8,807 Kcal / g.
Buharlaşma ısı
30 ºC'de 89.8 cal / g.
Yüzey gerilimi
20.0 ° C'de 17.06 din / cm.
İyonlaşma potansiyeli
9.53 eV.
Koku eşiği
0,83 ppm (saflık verilmez).
Kırılma indeksi
15 ºC'de 1.355.
edinme
Etil alkolden
Etil eter, katalizör olarak sülfürik asit varlığında etil alkolden elde edilebilir. Sulu bir ortamdaki sülfürik asit, hidronyum iyonu, H üreten ayrışır3Ey+.
Susuz etil alkol, etil alkol moleküllerinin protonasyonunu sağlayarak, 130 ° C ila 140 ° C arasında ısıtılan sülfürik asit çözeltisinden akar. Daha sonra, protonlanmamış etil alkolün bir başka molekülü protonlanmış molekül ile reaksiyona girer..
Bu olduğunda, ikinci etil alkol molekülünün nükleofilik saldırısı, birinci molekülden (protonlanmış olan) suyun salınmasını teşvik eder; sonuç olarak protonlanmış bir etil eter oluşur (CH3CH2OHCH2CH3) kısmen yüklü oksijen pozitif.
Bununla birlikte, bu sentez metodu verimi yitirir, çünkü sülfürik asit proseste üretilen su ile seyreltilir (etil alkol dehidrasyonunun ürünü).
Reaksiyonun sıcaklığı kritiktir. 130 ° C'nin altındaki sıcaklıklarda, reaksiyon yavaştır ve çoğunlukla etil alkol damıtılır.
150 ° C'nin üstünde, sülfürik asit, etil eter oluşturmak üzere etil alkolle birleşmek yerine etilen (çift bağ alken) oluşumuna neden olur.
Etilen'den
Tersine işlemde, etilenin buhar fazındaki hidrasyonu, etil eter, etil alkole ek olarak bir yan ürün olarak oluşturulabilir. Aslında, bu sentetik yol bu organik bileşiğin çoğunu üretir.
Bu işlem, daha fazla eter üretmek üzere ayarlanabilen katı bir desteğe sabitlenmiş fosforik asit katalizörleri kullanır.
Etanolün buhar fazında alümina katalizörleri varlığında susuz kalma, etil eter üretiminde% 95 verim verebilir.
toksisite
Cilt ve gözlerde tahrişe neden olabilir. Cilt ile teması kurumasına ve çatlamasına neden olabilir. Eter genellikle cilde nüfuz etmez, çünkü hızla buharlaşır..
Eterin neden olduğu gözlerin tahrişi genellikle hafiftir ve ciddi tahriş olması durumunda, hasar genellikle geri dönüşümlüdür.
Yutulması narkotik etkiler ve mide tahrişine neden olur. Şiddetli yutulması böbrek hasarına neden olabilir.
Eterin solunması burun ve boğazda tahrişe neden olabilir. Eterin solunması durumunda oluşabilir: uyuşukluk, heyecan, baş dönmesi, kusma, düzensiz solunum ve artan tükürük salgısı.
Yüksek maruz kalma bilinç kaybına ve hatta ölüme neden olabilir.
OSHA, 8 saatlik vardiyada ortalama 800 ppm mesleki maruziyet sınırı belirler.
Göz tahrişi seviyeleri: 100 ppm (insan). Göz tahrişi seviyeleri: 1200 mg / m3 (400 ppm).
uygulamaları
Organik çözücü
Brom, iyot ve diğer halojenleri çözmek için kullanılan organik bir çözücüdür; lipidlerin (yağlar), reçinelerin, saf kauçukların, bazı alkaloitlerin, zamkların, parfümlerin, selüloz asetat, selüloz nitrat, hidrokarbon ve boyaların çoğunluğu.
Ek olarak, hayvansal dokuların ve bitkilerin aktif prensiplerinin çıkarılmasında kullanılır, çünkü sudan daha düşük bir yoğunluğa sahiptir ve üzerinde yüzer ve istenen maddeleri eter içinde çözünmüş halde bırakır.
Genel anestezi
Terapötik bir avantaja sahip olmak için kloroformun yerine 1840'tan beri genel bir anestezik olarak kullanılmıştır. Bununla birlikte, yanıcı bir maddedir ve bu nedenle klinik ortamlarda kullanımı için ciddi zorluklarla karşılaşır..
Ek olarak, hastalarda bulantı ve kusma gibi istenmeyen bazı postoperatif yan etkiler ortaya çıkarır.
Bu nedenlerden ötürü eter genel bir anestezik olarak kullanılmaya başlandı, bunun yerine halotan gibi diğer anestezikler kullanıldı..
Eterin Ruhu
Etanol ile karıştırılmış eter, mide düzlüğü ve daha hafif gastralji formlarının tedavisinde kullanılan eter ruhu adı verilen çözeltiyi oluşturmak için kullanıldı..
Kan dolaşımının değerlendirilmesi
Eter bir kol ve akciğerler arasındaki kan dolaşımını değerlendirmek için kullanılmıştır. Eter bir kana enjekte edilir, kanı sağ atriyuma, sonra sağ ventriküle ve oradan akciğerlere getirir..
Eterin enjeksiyonundan, ekshale edilen havada eter kokusunun alınmasına kadar geçen süre yaklaşık 4 ila 6 saniyedir..
Öğretim laboratuvarları
Eter, laboratuvarlarda birçok deneyde öğretimde kullanılır; örneğin Mendel'in genetik yasalarının gösterilmesinde.
Eter, Drosophila cinsinin sineklerini uyuşturmak ve genetik yasalarını kanıtlamak için aralarında gerekli geçişlere izin vermek için kullanılır.
referanslar
- Graham Solomons T.W., Craig B. Fryhle. (2011). Organik Kimya Aminler. (10inci baskı.). Wiley Plus.
- Carey F. (2008). Organik Kimya (Altıncı baskı). Mc Graw Hill.
- Sevier (2018). Dietil eter. Doğrudan Bilim. Şu kaynaktan alındı: sciencedirect.com
- Ansiklopedi Britannica Editörleri. (2018). Etil eter. Britannica ncyclopædia. Alınan: britannica.com
- PubChem (2018). Eter. Alınan: pubchem.ncbi.nlm.nih.gov
- Vikipedi. (2018). Dietil eter. Alınan: en.wikipedia.org
- Güvenlik sayfası XI: etil eter. [PDF]. Alınan bilgiler: quimica.unam.mx


