Sabunlaşma Reaksiyonu ve Elde Edilebilecek Maddeler
sabunlaşma Bir esterin bazik hidrolizidir. Bu, esterin bir bazla (NaOH veya KOH) reaksiyona girmeyerek reaksiyona girmesi, alkol ve karboksilatların sodyum veya potasyum üretilmesi anlamına gelir. Kelime "sabun üretimi" anlamına gelir ve aslında, insanlık tarafından kullanılan en eski kimyasal reaksiyonlardan biridir..
Babil döneminde, odun ve bitkilerden ve hayvansal yağlardan toplanan küllerin yardımıyla, sabun yapma sanatını mükemmelleştirdiler. Neden hayvansal yağ? Bunun nedeni, gliserol denemeleri (trigliseritler) açısından zengin olmasıdır ve odun külleri, temel metal olan potasyum kaynağıdır..
Aksi takdirde, reaksiyon daha düşük bir verim verir, ancak boyalar ve bazı yüzeyler üzerindeki etkilerini yansıtacak kadar. Bu, pigmentlerin yağ ile karıştırıldığı yağlı boya durumlarıdır (ester kaynağı)..
indeks
- 1 Sabunlaşma reaksiyonu
- 1.1 Mekanizması
- 1.2 Kinetik
- 2 Sabunlaştırma ile elde edilebilecek maddeler
- 2.1 Sabunların çözücü etkisi
- 3 Kaynakça
Sabunlaşma reaksiyonu
mekanizma
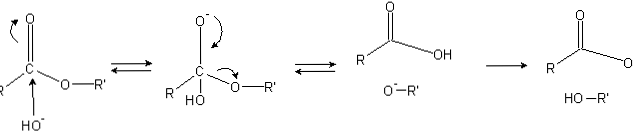
Esterler, OH gibi nükleofilik ataklara duyarlı bir asil grubuna (O = C-R) sahiptir.-.
Oksijen atomları, karbon atomundan elektronik yoğunluğu "çaldığı" için, ester durumunda, kısmen yüklüdür..
Sonuç olarak, bu pozitif yük meydana gelen nükleofilik atak ile (görüntünün sol tarafı) karbon atomuna elektron tedarik edebilen negatif türleri çeker. Sonuç olarak, bir tetrahedral ara madde (soldan sağa ikinci molekül) oluşur..
Dörtyüzlü ara maddenin oksijeni üzerindeki negatif yük, bir OH'nin ürünüdür.- Çevredeki. Daha sonra, bu negatif yük karbonil grubunun menşeli olması, daha sonra C-OR 'bağının kırılması için "zorlanması" için yerinden çıkar. Ayrıca, bu yer değiştirme bir karboksilik asit RCOOH ve bir alkokksit iyonu R'O üretir.-.
Son olarak, reaksiyon ortamı bazik olduğu için, alkokksit bir su molekülünü deprotonlar ve karboksilik asit başka bir OH ile reaksiyona girer.- sabunlaşma ürünleri üreten besiyerinin.
kinetik
Sabunlaşma reaksiyonunun hızı, reaktanların konsantrasyonlarıyla orantılıdır. Başka bir deyişle, ester (RCOOR ') veya baz (NaOH) konsantrasyonunu artırarak, reaksiyon daha yüksek bir hızda ilerleyecektir..
Bu ayrıca şu şekilde çevrilmiştir: sabunlaşma oranı, estere göre birinci sırada, tabanda da birinci sıradadır. Yukarıdaki, aşağıdaki matematiksel denklem ile ifade edilebilir:
Hız = k [RCOOR '] [NaOH]
K, sıcaklık veya basıncın bir fonksiyonu olarak değişen sabit veya hız katsayısıdır; yani, sıcaklık yükseldikçe, sabunlaşma hızı da artar. Bu nedenle besiyeri kaynamaya maruz kalıyor.
Her iki reaktif de birinci dereceden kinetik olduğundan, genel reaksiyon ikinci derecedendir..
Sabunlaşma reaksiyon mekanizmasında, tetrahedral ara maddenin oluşumu hem ester hem de baz içeren nükleofilik atak gerektirir.
Böylece, ikinci dereceden kinetik bu gerçeğe yansır, çünkü bunlar reaksiyonun (yavaş) belirleyici adımına müdahale ederler..
Sabunlaşma ile elde edilebilecek maddeler

Sabunlaşma ana ürünleri alkoller ve karboksilik asitlerin tuzlarıdır. Bir asit ortamında, yağ asitleri olarak bilinen yağların ve yağların sabunlaştırılmasıyla elde edilen ilgili RCOOH elde edilir..
Bu şekilde, sabunlar sabunlaştırmadan kaynaklanan yağ asitlerinin tuzlarından oluşur. Hangi katyonlarla çıkıyorsunuz? Na olabilirler+, K+, mg2+, inanç3+, vs.
Bu tuzlar suda çözünür, ancak sabunu kurutan ve sulu fazdan ayıran, karışıma eklenen NaCl etkisiyle çökeltilir. Bir trigliserit için sabunlaşma reaksiyonu aşağıdaki gibidir:
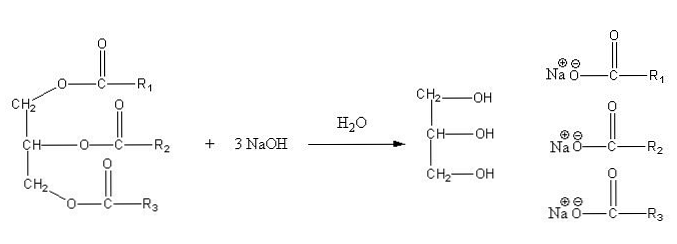
Gliserin, alkolik "E" dir ve sabun, ortaya çıkan yağ asitlerinin tüm tuzlarıdır. Burada, her sidechain -R farklı uzunluklara ve doymamışlık derecesine sahiptir. Sonuç olarak, bu zincirler yağlar ve bitkisel yağlar arasında fark yaratır.
Sabun üretiminin anahtarı, en iyi yağların ve yağların seçiminde ya da daha spesifik olarak, farklı trigliserit kaynaklarının seçiminde yatmaktadır..
Bu beyaz sabunlu kütle, yapısında boyalar ve diğer organik bileşikler içerebilir, hoş aroma ve parlak renkler verir. Buradan itibaren, olasılıklar bu ticarette sanat ve meslek ile doludur.
Bununla birlikte, sabunlaşma reaksiyonu ayrıca mutlaka gliserin veya sabunla yapmak zorunda kalmaması gereken sentetik bir karboksilik asit ve alkol yoludur..
Örneğin, basit etil asetat gibi herhangi bir esterin bazik hidrolizi, asetik asit ve etanol üretecektir.
Sabunların çözücü etkisi

Yağ asitlerinin tuzları suda çözünür, ancak iyonların çözüldüğü şekilde değildir; yani, sulu bir küre ile çevrilidir. Sabunlar söz konusu olduğunda, yan zincirleri -R teorik olarak suda çözülmelerini önler..
Bu nedenle, bu enerjisel olarak rahatsız edici bu pozisyona karşı koymak için, kutup başları, son (-COO) iken, kutupsal kafalar bir uç kutuplu organik çekirdek oluşturacak şekilde bu zincirlerle temas edecek şekilde yönlendirilirler- na+), su molekülleri ile etkileşime girerek "kutupsal kabuk" oluştur.
Yukarıdakiler misel olarak bilinen bu tip bir yapının gösterildiği yukarıdaki resimde gösterilmiştir..
"Siyah kuyruklar", gri küreler tarafından korunan organik bir çekirdekte dolaşmış hale gelen hidrofobik zincirlere karşılık gelir. Bu gri küreler kutup kalkanı, başları oluşturur -COO- na+.
Daha sonra, miseller, yağ asitlerinin tuzlarının kümeleridir (kümeleri). Bunlar içinde apolar karakterlerinden dolayı suda çözünmeyen yağları içine alabilirler..
Bunu nasıl yapıyorlar? Hem yağ hem de -R zincirleri hidrofobiktir, bu nedenle her ikisi de birbirleri için büyük bir yakınlığa sahiptir..
Miseller yağları içine aldığında, su polar kabukla etkileşime girerek sabunun çözünürlüğünü sağlar. Benzer şekilde, miseller negatif olarak yüklenir, birbirlerine itmelere neden olur ve bu nedenle yağın dağılmasını sağlar.
referanslar
- Anne Marie Helmenstine, Ph.D. (3 Ekim 2017). Sabunlaşma tanımı ve reaksiyonu. 24 Nisan 2018'de alındı, nereden: thoughtco.com
- Francis A. Carey. Organik Kimya Karboksilik asitler. (altıncı baskı, s. 863-866). Mc Graw Hill.
- Graham Solomons T.W., Craig B. Fryhle. Organik Kimya Lipids (10. basım, Sayfa 1056-1058). Wiley Plus.
- Vikipedi. (2018). Sabunlaşma. 24 Nisan 2018'de alındı, en.wikipedia.org adresinden alındı.
- Boyd C. (27 Şubat 2015). Sabunun kimyasını ve tarihini anlayın. 24 Nisan 2018 tarihinde alındı: chemservice.com
- Luca Laghi (27 Mart 2007). Sabunlaşma. 24 Nisan 2018'de, şu kaynaktan alındı: commons.wikimedia.org
- Amanda Crochet (12 Mayıs 2015). Micelle (gri tonlamalı). 24 Nisan 2018'de, şu kaynaktan alındı: commons.wikimedia.org


