Boyle-Mariotte Tarihi Kanunu, matematiksel anlatım, örnekler
Kanunu Boyle bir gaz tarafından veya üzerine uygulanan basınç ile işgal ettiği hacim arasındaki ilişkiyi ifade eden; gazın sıcaklığını ve miktarını (mol sayısı) sabit tutmak.
Bu yasa, Charles, Gay-Lussac, Charles ve Avogadro ile birlikte, ideal bir gazın davranışını açıklar; özellikle, mekanik bir kuvvet tarafından uygulanan hacim değişikliklerine tabi kapalı bir kapta.
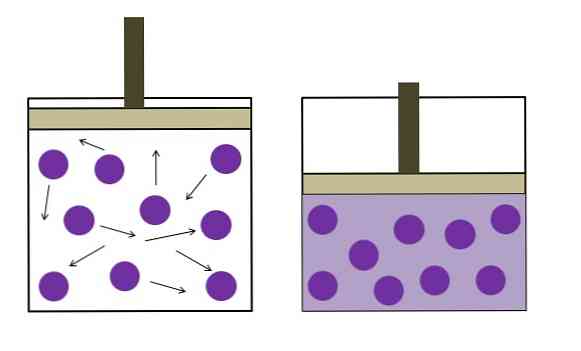
Yukarıdaki resim, Boyle-Mariotte yasasını kısaca özetlemektedir..
Mor noktalar kabın iç duvarlarıyla (solda) çarpışan molekülleri veya gaz atomlarını temsil eder. Bu gaz tarafından kullanılan kabın kullanılabilir alanını veya hacmini azaltarak çarpışmalar artar, bu da basınçta bir artışa (sağa) dönüşür..
Bu, kabın hava geçirmez şekilde kapatılması durumunda gazın P basıncının ve V hacminin ters orantılı olduğunu gösterir; Aksi takdirde, daha yüksek bir basınç kabın daha büyük bir genişlemesine eşit olacaktır.
Eğer P'ye karşı bir arsa V yapılmışsa, sırasıyla Y ve X eksenlerinde V ve P'nin verileriyle, bir asimptotik eğri gözlenecektir. V ne kadar küçük olursa, P'deki artış o kadar büyük olur; yani, eğri, X eksenindeki yüksek P değerlerine uzanacaktır..
Tabii ki, sıcaklık sabit kalır; ancak, aynı deney farklı sıcaklıklarda gerçekleştirildiyse, bu eğrilerin V vs P'nin nispi pozisyonları Kartezyen ekseninde değişecektir. Değişim, üç boyutlu bir eksende çizilirse, Z ekseninde sabit T olacak şekilde daha da belirginleşirdi..
indeks
- 1 Boyle yasasının tarihi
- 1.1 Arkaplan
- 1.2 Cıva ile deneme
- 1.3 Edme Mariotte
- 1.4 Yasanın güçlendirilmesi
- 2 Bu yasa neyi içerir??
- 3 Matematiksel anlatım
- 4 Ne için? Boyle yasası hangi sorunları çözer??
- 4.1 Buhar makineleri
- 4.2 Sip içecekler
- 4.3 Solunum sistemi
- 5 Örnekler (deneyler)
- 5.1 Deney 1
- 5.2 Deney 2
- 6 Kaynakça
Boyle yasasının tarihi
fon
Bilim adamı Galileo Galilei, boşluğun varlığına (1638) olan inancını ifade ettiğinden, bilim adamları havanın ve kısmi boşlukların özelliklerini incelemeye başladı..
İngiliz-İrlandalı kimyager Robert Boyle, 1638'de bir Alman mühendis ve fizikçi olan Otto von Guericke'nin bir hava pompası yaptırdığını öğrendikten sonra hava özellikleri çalışmasına başladı..
Cıva ile deneme
Boyle, hava basıncı çalışmalarını yürütmek için "J" şeklinde bir cam tüp kullandı ve yapımı Boyle'nin asistanı Robert Hooke'ye atfedildi. Kısa kolun ucu kapatıldı, tüpün uzun kolunun ucu cıva yerleştirmek için açıktı.
Boyle, başından beri havanın esnekliğini niteliksel ve niceliksel olarak incelemek istedi. "J" şeklindeki borunun açık ucundan cıva dökülerek, Boyle borunun kısa kolundaki havanın cıva basıncı altında daraldığı sonucuna varmıştır..
sonuçlar
Boruya eklenen cıva miktarı arttıkça, havaya uygulanan basınç da artar ve hacmi düşer. Boyle, basıncın bir fonksiyonu olarak negatif üstel tipte bir hava hacmi grafiği elde etti..
Eğer havanın hacmini basıncın tersine doğru çizerseniz, düz bir pozitif eğim çizginiz olur..
1662'de Boyle, iki değişkenin işlevsel bağımlılığını gösteren bir denklem şeklinde verilen ilk fiziksel yasayı yayınladı. Bu durumda, basınç ve hacim.
Boyle, bir gaza uygulanan basınç ile o gazın işgal ettiği hacim arasında ters bir ilişki olduğunu belirtti, bu oran gerçek gazlar için nispeten doğruydu. Çoğu gaz, orta derecede basınç ve sıcaklıklarda ideal gazlar gibi davranır..
Yüksek basınç ve düşük sıcaklıkla, ideallerin gerçek gazlarının davranışından sapmalar daha belirgin hale geldi..
Edme Mariotte
Fransız fizikçi Edme Mariotte (1620-1684) bağımsız olarak 1679'da aynı yasayı keşfetti. Bu yüzden Mariotte Yasası ya da Boyle's ve Mariotte Yasası denir..
Yasanın güçlendirilmesi
Daniel Bernoulli (1737), bir gaz basıncının, onu içeren kabın duvarları üzerindeki gaz parçacıklarının etkisiyle üretildiğine işaret ederek Boyle Yasasını güçlendirmiştir..
1845'te John Waterston, gazların kinetik teorisinin temel prensiplerine odaklandığı bilimsel bir makale yayınladı..
Daha sonra, Rudolf Clausius, James Maxwell ve Ludqwig Boltzmann, gazın kinetik gaz teorisini, gazın uyguladığı basıncı, hareket halindeki gaz parçacıklarının hızı ile ilişkilendirdi..
Bir gaz içeren kabın hacmi ne kadar küçükse, kabın duvarlarına karşı oluşturan parçacıkların çarpma sıklığı da o kadar yüksek olur; ve bu nedenle, gaz tarafından uygulanan basınç arttıkça.
Bu yasa neyi içerir??
Boyle tarafından yapılan deneyler, bir gazın işgal ettiği hacim ile bunun üzerine uygulanan basınç arasında ters bir ilişki olduğunu göstermektedir. Bununla birlikte, yukarıda bahsedilen ilişki Boyle'ye atfedilen basınca göre bir hacim değişim grafiği ile belirtildiği gibi tamamen doğrusal değildir..
Boyle Yasası'nda, bir gazın işgal ettiği hacmin, basınçla ters orantılı olduğu belirtiliyor. Ayrıca, bir gazın hacminin hacminin sabit olduğu ürünün sabit olduğu belirtilmektedir..
Matematiksel anlatım
Boyle-Mariotte kanununun matematiksel ifadesine ulaşmak için:
V α 1 / P
Bir gaz tarafından kullanılan hacmin basıncı ile ters orantılı olduğunu gösterir. Ancak, bu ilişkinin ne kadar ters orantılı olduğunu belirleyen bir sabit var.
V = k / P
Burada k, orantılığın sabitidir. Sahip olduğunuz k temizliği:
VP = k
Bir gazın hacmine göre hacminin sabiti sabittir. o zaman:
V1P1 = k ve V2P2 = k
Ve bundan şöyle çıkarılabilir:
V1P1 = V2P2
İkincisi, Boyle yasasının son ifadesi veya denklemidir..
Bu ne için? Boyle yasası hangi sorunları çözer??
Buhar makineleri

Boyle-Mariotte Kanunu, buhar motorlarının çalışması için geçerlidir. Termal enerjinin bir miktar sudan mekanik enerjiye dönüşümünü kullanan harici bir yanmalı motordur..
Su, hava geçirmez bir şekilde kapatılmış bir kazan içerisinde ısıtılmakta ve üretilen buhar, bir pistonu iterek silindirin hacim genişlemesini üreten Boyle-Mariote yasasına göre bir basınç uygulamaktadır..
Pistonun doğrusal hareketi, bir lokomotifin tekerleklerini veya bir elektrik jeneratörünün rotorunu çalıştırabilen bir krank ve krank sistemi kullanılarak, dönme hareketine dönüştürülür..
Şu anda, alternatif buhar motoru az kullanılmış bir motordur, çünkü taşıt araçlarında elektrik motoru ve içten yanmalı motor tarafından yerinden edilmiştir..
İçecekleri yudumlarken
Plastik bir tüp vasıtasıyla bir şişeden bir alkolsüz içecek veya meyve suyu emme eylemi, Boyle-Mariotte yasası ile ilgilidir. Ağız kullanılarak hava tüpten emildiğinde, tüpün içindeki basınçta bir düşüş olur..
Bu basınç düşüşü tüpün içindeki sıvının yukarı doğru hareketini kolaylaştırarak içeri girmesine izin verir. Bu aynı prensip, bir şırınga kullanarak kanın çıkarılmasında çalışır..
Solunum sistemi
Boyle-Mariotte yasası, solunum sisteminin işleyişi ile yakından ilgilidir. İlham aşamasında diyaframın ve diğer kasların kasılması meydana gelir; örneğin, göğüs kafesinin bir genişlemesini üreten harici interkostallar.
Bu, intrapleural basınçta bir azalmaya neden olur ve bu, akciğer hacminde bir artışa neden olan bir akciğer genişlemesine neden olur. Bu nedenle intrapulmoner basınç, Boyle-Mariotte yasasında belirtilenlere göre azalır..
İntrapulmoner basınç atmosferik olmayan olduğunda, atmosferik hava akciğerlere akar ve bu da ciğerlerde artan basınçla sonuçlanır; atmosfer basıncına baskısını eşitlemek ve ilham fazını sonlandırmak.
Daha sonra, inspirasyon kasları gevşer ve ekspiratuar kaslar büzülür. Ek olarak, Boyle-Mariotte yasası ile açıklanabilen intrapulmoner basınçta bir artış ile sonuçlanan, akciğer hacminde bir azalmaya neden olan bir olgu olan pulmoner elastik retraksiyonu meydana gelir..
İntrapulmoner basıncı artırarak ve atmosferik basınçtan daha büyük hale gelince, hava akciğerlerin içinden atmosfere akar. Bu, basınç eşitlenene kadar gerçekleşir, bu da son kullanma aşamasını sonuçlandırır..
Örnekler (deneyler)
1. Deneme
Küçük bir balon sıkıca kapalı olarak yerleştirilmiş olup, ağzına, pistonun çıkarıldığı bir şırınganın içine yaklaşık 20 ml'lik bir düğüm atılmıştır. Şırınganın pompası, şırınganın orta kısmına doğru yerleştirilir, iğne çıkarılır ve hava girişi tıkanır.
gözlem
Enjektörün pistonunu yavaşça çekerek balonun şişirildiği gözlenir..
açıklama
Balonun duvarına iki basınç uygulanır: iç yüzünde bir basınç, balonun içinde bulunan havanın ürünü ve balonun dış tarafında, şırınganın içinde bulunan havanın uyguladığı başka bir basınç..
Enjektörün pistonunu çekerken, içinde yarım bir vakum oluşur. Bu nedenle, pompa duvarının dış yüzeyindeki hava basıncı azalır, böylece pompa içine uygulanan basınç nispeten daha büyük olur..
Boyle-Mariote yasalarına göre, bu net basınç balon duvarının bir miktarını ve balon hacminde bir artışa neden olacaktır..
2. Deneme
Kesimin mümkün olduğu kadar yatay olduğundan emin olarak, yaklaşık olarak ikiye kadar plastik bir şişe kesin. Şişenin ağzına iyi ayarlanmış bir balon yerleştirilir, aynı zamanda derin bir kaba belirli miktarda su konur..
gözlem
Şişenin dibini balon ile yemeğin suyuna yerleştirerek, balon orta derecede şişirilir..
açıklama
Su, şişenin duvarındaki ve balonun içindeki havanın basıncını artırarak belirli bir havanın yerini alır. Bu, Boyle-Mariotte yasalarına göre, dünyadaki enflasyonun görselleştirdiği, dünya hacminde bir artışa neden oluyor.
referanslar
- Vikipedi. (2019). Boyle kanunu. Alınan: en.wikipedia.org
- Ansiklopedi Britannica Editörleri. (27 Temmuz 2018) Boyle kanunu. Ansiklopedi Britannica. Alınan: britannica.com
- Helmenstine, Todd. (5 Aralık 2018). Boyle Yasası Formülü. Alınan adres: thoughtco.com
- Genç Hint Filmleri. (15 Mayıs 2018). Boyle Yasası: Çocuklar İçin Bilim Deneyi. Şu kaynaktan alındı: yifindia.com
- Cecilia Bembibre (22 Mayıs 2011). Sıcak hava balonu ABC tanımı. Definicionabc.com'dan alındı
- Ganong, W, F. (2003). Tıbbi Fizyoloji (19. Baskı). Editoryal Modern El Kitabı.


