Kimyasal Hibridizasyon sp, sp2, sp3
kimyasal hibridizasyon Valencia Link'in Teorisinin (TEV) teorisindeki kusurları kapsayacak şekilde kavramı kimyager Linus Pauling tarafından 1931'de tanıtılan atomik yörüngelerin "karışımı" dır. Hangi kusurlar? Bunlar: moleküler geometriler ve metan (CH) gibi moleküllerdeki eşdeğer bağlantı uzunlukları4).
TEV'e göre, metanda, C'nin atomik yörüngeleri, dört H atomlu dört σ bağı oluşturur, C'nin forma formlu (alt görüntü) 2p yörüngeleri birbirine diktir, bu nedenle Hs birbirinden ayrılmalıdır. 90º açıyla başkalarının.
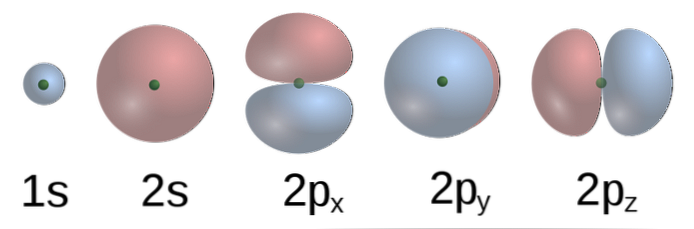
Ek olarak, C'nin 2s (küresel) yörüngesi, H'nin 1s yörüngesine, diğer üç Hs'ye göre 135 ° 'lik bir açıyla bağlanmıştır, ancak, deneysel olarak CH'deki açıların deneysel olarak bulunmuştur.4 109.5º'dir ve buna ek olarak, C-H bağlarının uzunlukları eşdeğerdir..
Bunu açıklamak için, orijinal atomik orbitallerin bir kombinasyonunun (dejenere) dört dejenere hibrit orbital oluşturduğu düşünülmelidir. İşte kimyasal kimya geliyor. Hibrit orbitaller nasıldır? Bu onları üreten atomik yörüngelere bağlıdır. Ayrıca, bunların elektronik özelliklerinin bir karışımını sergilerler..
indeks
- 1 sp3 Hibridizasyon
- 1.1 Yorumlama
- 1.2 Bağlantı açılarının sapmaları
- 2 Hibridizasyon sp2
- 3 Hibridizasyon sp
- 4 Kaynakça
Hibridizasyon sp3
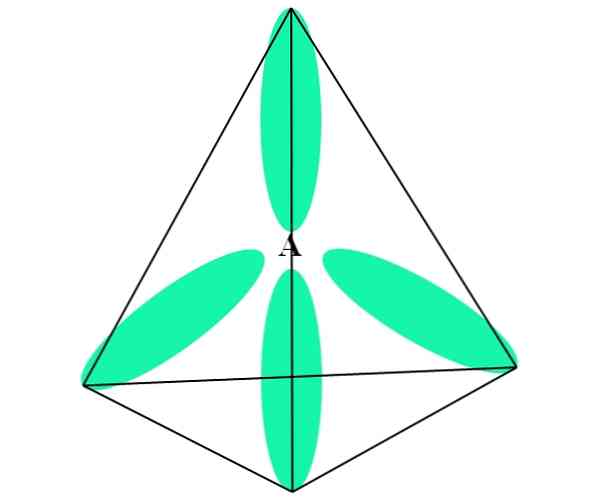
CH durumunda4, C'nin hibridizasyonu sp3. Bu yaklaşımdan, moleküler geometri dört sp orbital ile açıklanmıştır.3 109.5º de ayrılmış ve bir tetrahedronun köşelerine dönük.
Yukarıdaki resimde sp orbitallerinin nasıl olduğunu görebilirsiniz3 (yeşil) atomun etrafında bir dörtyüzlü elektronik ortam oluşturur (A, CH için C'dir)4).
Neden 109.5º ve farklı bir geometriyi çizmek için diğer açılardan değil? Bunun nedeni, bu açının A'ya bağlı dört atomun elektronik itişlerini en aza indirmesidir..
Bu şekilde, CH molekülü4 bir tetrahedron (tetrahedral moleküler geometri) olarak temsil edilebilir.
H yerine, C diğer atom gruplarıyla bağlantılar oluşturduysa, hibridizasyonu ne olurdu? Karbon dört σ bağı (C-A) oluşturduğu sürece hibridizasyonu3.
CH gibi diğer organik bileşiklerde olduğu varsayılabilir.3OH, CCİ4, C (CH)3)4, C6'H12 (sikloheksan), vb., karbonun bir sp hibridizasyonu vardır3.
Bu, basit bağlara sahip karbonların ayrışma noktalarını temsil ettiği organik yapıları çizmek için temeldir; yani, yapı tek bir düzlemde kalmaz.
yorumlama
Bu hibrit yörüngeler için matematiksel yönlere değinmeden (dalga fonksiyonları) en basit yorum nedir? Sp orbitalleri3 bunların dört yörünge tarafından kaynaklandığını belirtir: bir s ve üç p.
Çünkü bu atomik orbitallerin kombinasyonunun ideal olması gerekiyordu, dört sp orbital3 sonuç aynıdır ve uzayda farklı yönelimler işgal eder (örneğin orbitaller px, pve ve pz).
Yukarıdakiler, olası hibritleşmelerin geri kalanı için geçerlidir: Oluşan hibrit orbitallerin sayısı, birleşik atomik orbitallerinkiyle aynıdır. Örneğin, sp melez orbitaller3d2 altı atomik yörüngeden oluşurlar: bir s, üç p ve iki d.
Bağlantı açılarının sapmaları
Valensiya Katmanının Elektronik Çiftlerinin (VSEPR) İtme Teorisi'ne göre, bir çift serbest elektron, bağlı bir atomdan daha fazla hacim işgal eder. Bu, bağlantıların birbirinden ayrılmasına, elektronik gerginliğin azaltılmasına ve 109.5º açıların yönlendirilmesine neden olur:
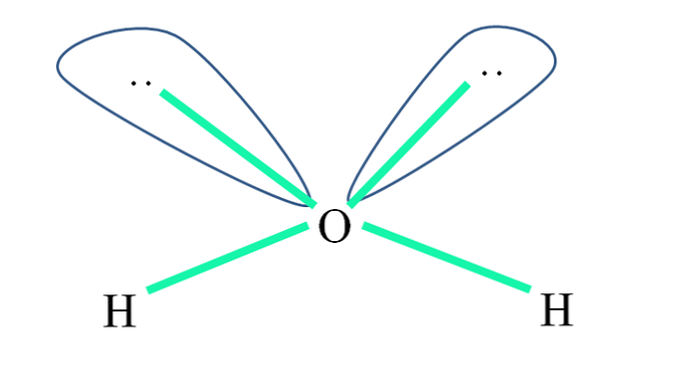
Örneğin, su molekülünde H atomları sp orbitallerine bağlanır3 (yeşil) ve ayrıca paylaşılmayan elektron çiftleri ":" bu orbitalleri işgal eder.
Bu elektron çiftlerinin itmeleri genellikle hacimleri nedeniyle σ O-H bağlarını iterek iki gözü olan "gözle iki küre" olarak temsil edilir..
Bu nedenle, sudaki bağlantı açıları tetrahedral geometri için beklenen 109,5º yerine gerçekten 105º'dir..
H hangi geometriye sahiptir?2Ç? Açısal bir geometriye sahiptir. Neden? Çünkü elektronik geometri dört yüzlü olmasına rağmen, iki çift paylaşılmayan elektron ondan açısal moleküler bir geometriye dönüşür..
Hibridizasyon sp2
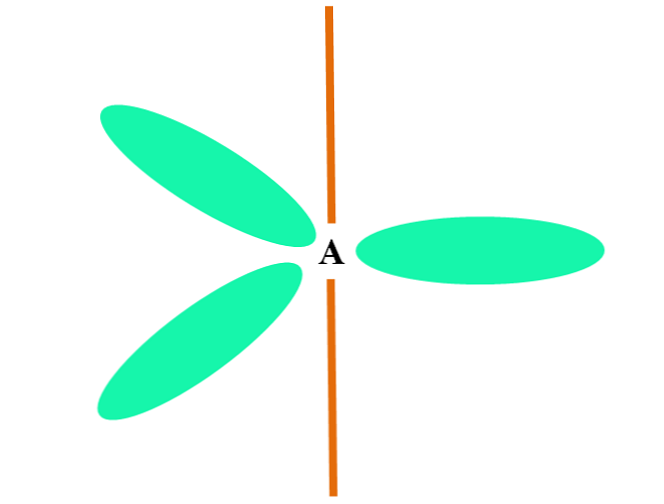
Bir atom iki p ve bir s orbitalini birleştirdiğinde, üç sp hibrid orbital üretir2; ancak, orbital bir p, yukarıdaki resimde turuncu bir çubuk olarak gösterilen (üç olduklarından) değişmeden kalır..
Burada, üç sp orbital2 turuncu çubuktan farklarını vurgulamak için yeşil: “saf” p orbital.
Sp hibridizasyonu olan bir atom2 düz trigonal bir zemin olarak görselleştirilebilir (sp orbitalleri ile çizilen üçgen2 (yeşil renkte), köşeleri 120 separated açılarla ayrılmış ve bir çubuğa dik.
Saf p orbitalin rolü nedir? Çifte bağ oluşturma (=). Sp orbitalleri2 saf p orbital a π bağ (üç ya da üçlü bağ bir ya da iki p bağ anlamına gelir) varken üç σ bağının oluşmasına izin verir.
Örneğin, karbonil grubunu ve formaldehit molekülünün yapısını çizmek (H2C = O), aşağıdaki gibi ilerler:
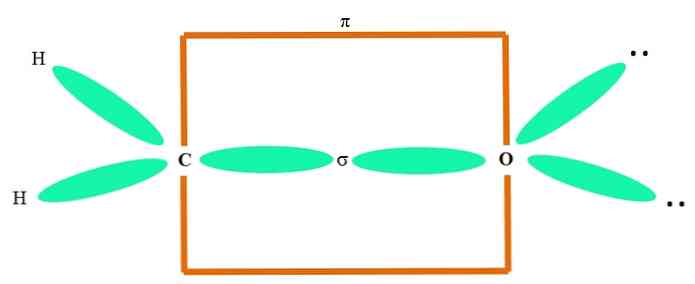
Sp orbitalleri2 C ve O'nun her ikisi de bir bağ σ, saf orbitalleri ise bir bağ π (turuncu dikdörtgen) oluşturur..
Elektronik grupların geri kalanının (H atomları ve paylaşılmayan elektron çiftleri) diğer sp orbitallerinde nasıl yer aldığı görülmektedir.2, 120º ile ayrılmış.
Hibridizasyon sp
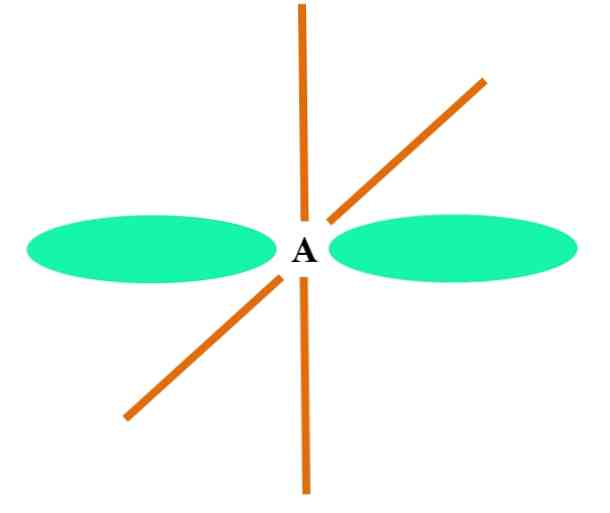
Üstteki görüntü, sp hibridizasyonu olan bir atom A'yı göstermektedir. Burada, bir yörünge s ve bir yörünge iki dejenere sp yörüngesini oluşturmak için birleşir. Bununla birlikte, şimdi iki saf p orbital değişmeden kalır, bu da A'nın iki çift bağ veya üçlü bir bağ oluşturmasına izin verir (≡).
Başka bir deyişle: eğer bir yapıda bir C yukarıdakilere uyuyorsa (= C = veya C≡C), o zaman hibridizasyonu sp. Diğer daha az açıklayıcı atomlar için - geçiş metalleri gibi - elektronik ve moleküler geometrilerin açıklaması karmaşıktır çünkü orbitaller d ve hatta f orbitalleri de göz önünde bulundurulur..
Hibrit orbitaller, 180 ° 'lik bir açıyla ayrılır. Bu nedenle bağlı atomlar doğrusal bir moleküler geometride (B-A-B) düzenlenir. Son olarak, aşağıdaki resimde siyanür anyonunun yapısını görebilirsiniz:

referanslar
- Sven. (3 Haziran 2006). S-p-orbitalleri. [Şekil]. 24 Mayıs 2018'de, commons.wikimedia.org adresinden alındı.
- Richard C. Banks. (Mayıs 2002). Yapıştırma ve Hibridizasyon. 24 Mayıs 2018'de, şu kaynaktan alındı: chemistry.boisestate.edu
- James. (2018). Bir Hibridizasyon Kısayolu. 24 Mayıs 2018'de alındı, masterorganicchemistry.com adresinden alındı
- Ian Hunt. Calgary Üniversitesi, Kimya Bölümü. sp3 hibridizasyonu. 24 Mayıs 2018'de alınan, chem.ucalgary.ca
- Kimyasal Bağlar II: Atomik Orbitallerin Moleküler Geometrisi ve Hibridizasyonu Bölüm 10. [PDF]. 24 Mayıs 2018'de alındı, wou.edu
- Quimitube. (2015). Kovalent bağ: Atomik orbitallerin melezleşmesine giriş. 24 Mayıs 2018 tarihinde alındı: quimitube.com
- Shiver ve Atkins. (2008). İnorganik kimya (Dördüncü baskı, sayfa 51). Mc Graw Hill.


