Kalsiyum fosfat (Ca3 (PO4) 2) yapısı, özellikleri, oluşumu ve kullanımları
kalsiyum fosfat kimyasal formülü Ca olan inorganik ve üçüncül bir tuzdur.3(PO4)2. Formül, bu tuzun bileşiminin sırasıyla kalsiyum ve fosfat için 3: 2 olduğunu belirtir. Bu, doğrudan Ca katyonunun gösterildiği alt resimde görülebilir.2+ ve anyon PO43-. Her üç Ca için2+ İki tane PO var43- onlarla etkileşime girme.
Öte yandan, kalsiyum fosfat, Ca / P oranına, ayrıca hidrasyon derecesine ve pH derecesine bağlı olarak değişen bir dizi tuz anlamına gelir. Aslında, var olan ve sentezlenebilen birçok kalsiyum fosfat türü vardır. Bununla birlikte, isimlendirmenin anlamını takiben, kalsiyum fosfat, sadece yukarıda belirtilen.

Ca dahil tüm kalsiyum fosfatlar3(PO4)2, Hafif grimsi tonlarda düz beyazdırlar. Granüler, ince, kristal olabilirler ve mikrometre etrafındaki parçacık boyutlarına sahip olabilirler; ve hatta, bu fosfatların nanoparçacıkları, kemikler için biyouyumlu malzemeler tasarlanan hazırlandı.
Bu biyouyumluluk, bu tuzların dişlerde ve kısaca memelilerin kemik dokularında bulunmasından kaynaklanmaktadır. Örneğin, hidroksiapatit, aynı tuzun amorf bir fazıyla etkileşime giren kristalimsi bir kalsiyum fosfattır..
Bu, amorf ve kristalin kalsiyum fosfatların var olduğu anlamına gelir. Bu nedenle, kalsiyum fosfatlara dayanan materyalleri sentezlerken çeşitlilik ve çoklu seçenekler şaşırtıcı değildir; Kemik restorasyonuna odaklanmak için dünya çapında mülk araştırmacıları her gün daha fazla ilgilenen malzemeler.
indeks
- 1 Kalsiyum fosfatın yapısı
- 1.1 Amorf kalsiyum fosfat
- 1.2 Ailenin geri kalanı
- 2 Fiziksel ve kimyasal özellikler
- 2.1 İsimler
- 2.2 Moleküler ağırlık
- 2.3 Fiziksel tanım
- 2.4 Tat
- 2.5 Erime noktası
- 2.6 Çözünürlük
- 2.7 Yoğunluk
- 2.8 Kırılma indisi
- 2.9 Standart eğitim entalpisi
- 2.10 Depolama sıcaklığı
- 2.11 pH
- 3 Eğitim
- 3.1 Kalsiyum nitrat ve amonyum hidrojen fosfat
- 3.2 Kalsiyum hidroksit ve fosforik asit
- 4 Kullanım
- 4.1 Kemik dokusunda
- 4.2 Biyoseramik Çimentolar
- 4.3 Doktorlar
- 4.4 Diğer
- 5 Kaynakça
Kalsiyum fosfatın yapısı
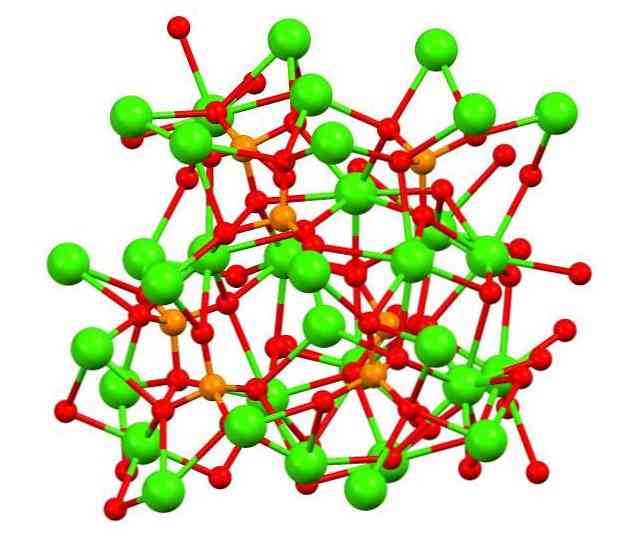
Üstteki resim, yabancı madde olarak magnezyum ve demir içerebilen garip beyaz lokosit mineralinde tribazik patiska fosfatın yapısını göstermektedir.
İlk bakışta karmaşık görünse de, modelin fosfatların oksijen atomları ve kalsiyum metal merkezleri arasında kovalent etkileşimler varsaydığını açıklığa kavuşturmak gerekir..
Temsil yoluyla geçerlidir, ancak etkileşimler elektrostatiktir; yani katyonlar Ca2+ PO anyonlarına ilgi duyulur43- (Ca2+- O-PO33-). Bunu akılda tutarak, görüntüdeki kalsiyumun (yeşil küreler) neden negatif yüklü oksijen atomları (kırmızı küreler) ile çevrili olduğu anlaşılmaktadır..
Çok fazla iyon olduğunda, simetrik bir düzenleme veya deseni görünür bırakmaz. Ca3(PO4)2 Düşük sıcaklıklarda kabul edilir (T<1000°C) una celda unitaria correspondiente a un sistema cristalino romboédrico; a este polimorfo se le conoce con el nombre de β-Ca3(PO4)2 (β-TCP, İngilizce kısaltması için).
Yüksek sıcaklıklarda ise, α-Ca polimorfuna dönüşür.3(PO4)2 (α-TCP), birim hücresi, monoklinik bir kristalli sisteme karşılık gelir. Daha da yüksek sıcaklıklarda, polimorf a'-Ca da oluşturulabilir.3(PO4)2, altıgen kristal yapılı olan.
Amorf kalsiyum fosfat
Bir tuzdan beklenebilecek kalsiyum fosfat için kristal yapılar belirtilmiştir. Bununla birlikte, tanımı gereği kristallerden ziyade bir tür "kalsiyum fosfat camına" bağlı, düzensiz ve asimetrik yapılar gösterme yeteneğine sahiptir..
Bu olduğunda, kalsiyum fosfatın amorf bir yapıya sahip olduğu söylenir (ACP)., amorf kalsiyum fosfat). Bazı yazarlar, Ca'nın biyolojik özelliklerinden sorumlu olan bu yapı tipine işaret eder.3(PO4)2 kemik dokularında onarımı ve biyomimetrasyonu mümkün.
Yapısının nükleer manyetik rezonans (NMR) ile açıklanması sayesinde OH iyonlarının varlığı tespit edilmiştir.- ve HPO42- ACP’de Bu iyonlar, fosfatlardan birinin hidrolizi ile oluşur:
PO43- + 'H2Ey <=> HPO42- + OH-
Sonuç olarak, ACP'nin gerçek yapısı daha karmaşık hale gelir, iyonları bileşimi formülle temsil edilir: Ca9(PO4)6-X(HPO4)x(OH)x. 'X', hidrasyon derecesini gösterir, çünkü x = 1 ise, formül şöyle olacaktır: Ca9(PO4)5(HPO4) (OH).
PCA'nın sahip olabileceği farklı yapılar Ca / P molar oranlarına bağlıdır; diğer bir deyişle, sonuçta elde edilen bileşimlerini değiştiren nispi miktarlarda kalsiyum ve fosfattır..
Ailenin geri kalanı
Kalsiyum fosfatlar aslen organik bir matris ile etkileşime girebilen inorganik bileşiklerin bir ailesidir..
Diğer fosfatlar kalsiyum eşliğinde anyonları değiştirerek "basit" elde edilir (PO43-, HPO42-, 'H2PO4-, OH-) ve ayrıca katıdaki yabancı maddelerin türü. Böylece, her biri kendi yapısı ve özelliklerine sahip on bir kalsiyum fosfat veya daha fazlası, doğal veya yapay olarak ortaya çıkabilir..
Aşağıda bazı fosfatlar ve bunlara ait yapılar ve kimyasal formüller bulunmaktadır:
-Hidrojen kalsiyum fosfat dihidrat, CaHPO4∙ 2H2O: monoklinik.
-Kalsiyum dihidrojen fosfat monohidrat, Ca (H)2PO4)2∙ H2O: üç tekerlekli.
-Susuz diasit fosfat, Ca (H)2PO4)2: üç tekerlekli.
-Ocalcium hidrojen fosfat (OCP), Ca8'H2(PO4)6: üç tekerlekli Hidroksiapatit sentezinde bir öncüdür.
-Hidroksiapatit, Ca5(PO4)3OH: altıgen.
Fiziksel ve kimyasal özellikler
isimler
-Kalsiyum fosfat
-Trikalsiyum fosfat
-Trikalsiyum difosfat
Moleküler ağırlık
310.74 g / mol.
Fiziksel açıklama
Kokusuz beyaz bir katıdır..
lezzet
tatsız.
Erime noktası
1670 ºK (1391 ºC).
çözünürlük
-Suda pratik olarak çözünmez.
-Etanolde çözünmez.
-Seyreltik hidroklorik asit ve nitrik asitte çözünür.
yoğunluk
3.14 g / cm3.
Kırılma indeksi
1629
Standart eğitim entalpisi
4126 kcal / mol.
Depolama sıcaklığı
2-8 ºC.
pH
Sulu süspansiyon içinde 6-8 g / L kalsiyum fosfat.
eğitim
Kalsiyum nitrat ve hidrojen amonyum fosfat
Kalsiyum fosfat üretmek veya oluşturmak için çok sayıda yöntem vardır. Bunlardan biri iki tuz karışımından oluşur, Ca (NO)3)2∙ 4H2O ve (NH4)2HPO4, Daha önce sırasıyla mutlak alkol ve su içinde çözüldü. Bir tuz kalsiyum ve diğer fosfat sağlar.
Bu karışımdan ACP çökelir, bu daha sonra 800 ° C'de ve 2 saat boyunca bir fırında ısıtmaya tabi tutulur. Bu işlem sonucunda β-Ca elde edilir.3(PO4)2. Sıcaklıkları, ajitasyon ve temas sürelerini dikkatlice kontrol ederek nanokristal oluşumu meydana gelebilir..
Polimorf α-Ca'yı oluşturmak için3(PO4)2 fosfatın 1000 ° C'nin üzerinde ısıtılması gerekir Bu ısıtma, bu polimorfu oda sıcaklığında kullanması için yeterince stabilize eden diğer metal iyonlarının varlığında gerçekleştirilir; yani, istikrarlı bir meta durumunda kalır.
Kalsiyum hidroksit ve fosforik asit
Kalsiyum fosfat ayrıca, kalsiyum hidroksit ve fosforik asit çözeltileri ile oluşan asit-baz nötrleştirme ile karıştırılarak da oluşturulabilir. Ana likörlerde yarım gün olgunlaştırılmasından ve uygun filtrasyonundan, yıkanmasından, kurutulmasından ve elenmesinden sonra, granül şekilsiz bir fosfat tozu elde edilir, ACP.
Bu ACP, aşağıdaki kimyasal denklemlere göre dönüşüm yaparak yüksek sıcaklıktaki ürünü reaksiyona sokar:
2Ca9(HPO4) (PO4)5(OH) => 2Ca9(P2Ey7)0.5(PO4)5(OH) + H2O (T = 446.60 ° C'de)
2Ca9(P2Ey7)0.5(PO4)5(OH) => 3Ca3(PO4)2 + 0.5 H2O (T = 748,56 ° C'de)
Bu şekilde β-Ca elde edilir.3(PO4)2, en yaygın ve kararlı polimorf.
uygulamaları
Kemik dokusunda
Ca3(PO4)2 Kemik külünün ana inorganik bileşenidir. Kemik replasmanının bir bileşenidir, bu kemikte bulunan minerallere kimyasal benzerliği ile açıklanmaktadır..
Kalsiyum fosfat biyomalzemeleri kemik kusurlarını düzeltmek ve titanyum metal protezlerinin kaplanmasında kullanılır. Kalsiyum fosfat üzerlerinde biriktirilir, ortamdan izole edilir ve titanyum korozyon sürecini yavaşlatır.
Ca dahil kalsiyum fosfatlar3(PO4)2, Seramik malzemelerin üretiminde kullanılırlar. Bu malzemeler biyo-uyumludur ve günümüzde periodontal hastalık, endodontik enfeksiyonlar ve diğer koşullardan kaynaklanan alveoler kemik kaybını restore etmek için kullanılmaktadır..
Bununla birlikte, kronik bakteriyel enfeksiyon bulunmayan alanlarda sadece periapikal kemik onarımını hızlandırmak için kullanılmaları gerekir..
Otojen bir kemik grefti kullanılması mümkün olmadığında kemik defektlerinin onarımında kalsiyum fosfat kullanılabilir. Tek başına veya poliglikolik asit gibi biyobozunur ve emilebilir bir polimer ile kombinasyon halinde kullanmak mümkündür.
Biyoseramik çimento
Kalsiyum fosfat çimentosu (CPC) kemik dokusunun tamirinde kullanılan bir başka biyoseramiktir. Farklı kalsiyum fosfat türlerinin tozunun suyla karıştırılması ve macun haline getirilmesiyle elde edilir. Macun enjekte edilebilir veya kemik defektine veya boşluğuna ayarlanabilir.
Çimentolar kalıplanır, yavaş yavaş emilir ve yeni oluşturulan kemik ile değiştirilir.
tıbbi
-Ca3(PO4)2 Bazik bir tuzdur, bu yüzden fazla mide asidini nötralize etmek ve pH'ı artırmak için bir antasit olarak kullanılır. Diş macununda, dişlerin ve kemik hemostazının remineralizasyon sürecini kolaylaştırmak için bir kalsiyum ve fosfat kaynağı sağlar.
-Kalsiyum yerine en ucuz yol karbonat ve sitrat kullanımı olsa da, besin takviyesi olarak da kullanılır..
-Kalsiyum fosfat, tetan, gizli hipokalsemi ve bakım tedavisi tedavisinde kullanılabilir. Ayrıca, hamilelik ve emzirme döneminde kalsiyum takviyesinde faydalıdır.
-Radyoaktif izotop radyo (Ra-226) ve stronsiyum (Sr-90) ile kirlenmenin tedavisinde kullanılır. Kalsiyum fosfat, sindirim kanalında radyoaktif izotopların emilimini engeller, böylece onların neden olduğu hasarı sınırlar..
diğerleri
-Kalsiyum fosfat kuşlar için bir yem olarak kullanılır. Ayrıca, diş macunlarında tartarı kontrol etmek için kullanılır..
-Topaklanma önleyici bir madde olarak kullanılır, örneğin sofra tuzunun sıkışmasını önlemek için.
-Un için ağartıcı olarak kullanılır. Domuz domuz yağı ise istenmeyen bir renklenmeyi önler ve kızartma durumunu iyileştirir.
referanslar
- Tung M.S. (1998) Kalsiyum Fosfatlar: Yapısı, Bileşimi, Çözünürlüğü ve Kararlılığı. In: Amjad Z. (ed) Biyolojik ve Endüstriyel Sistemlerde Kalsiyum Fosfatlar. Springer, Boston, MA.
- Langlang Liu, Yanzeng Wu, Chao Xu, Suchun Yu, Xiaopei Wu ve Honglian Dai. (2018). "Nano-β-Trikalsiyum Fosfatın Sentezi, Karakterizasyonu ve Hepatoselüler Karsinoma Hücrelerinde Önleme", Nanomalzemeler Dergisi, vol. 2018, Makale numarası 7083416, 7 sayfa, 2018.
- Combes, Mesih ve Rey, Hristiyan. (2010). Amorf kalsiyum fosfatlar: sentez, biyomalzemelerde özellikleri ve kullanımları. Acta Biomaterialia, vol. 6 (n ° 9). s. 3362-3378. ISSN 1742-7061
- Vikipedi. (2019). Trikalsiyum fosfat. Alınan: en.wikipedia.org
- Abida ve diğ. (2017). Trikalsiyum fosfat tozu: Hazırlama, karakterizasyon ve sıkıştırma yetenekleri. Akdeniz Kimya Dergisi 2017, 6 (3), 71-76.
- Pubchem. (2019). Kalsiyum fosfat. Alınan: pubchem.ncbi.nlm.nih.gov
- Elsevier. (2019). Kalsiyum fosfat. Doğrudan Bilim. Şu kaynaktan alındı: sciencedirect.com


