Su elektroliz prosedürü, teknikleri, ne için, ev deneyi
su elektrolizi Bir elektrik akımı uygulanarak suyun temel bileşenlerine ayrışmasıdır. İlerlerken, iki inert yüzeyde H ve hidrojen oksijen oluşuyor, H2 ve O2. Bu iki yüzey elektrot adıyla daha iyi bilinmektedir..
Teorik olarak H hacmi2 Oluşan hacminin iki katı olmalı2. Neden? Çünkü su molekülü, H'ye eşit bir H / O oranına, yani her oksijen için iki H'ye sahiptir. Bu ilişki doğrudan kimyasal formülü H ile kontrol edilir.2O. Ancak, birçok deneysel faktör elde edilen hacimleri etkiler.

Elektroliz suya batırılmış tüplerin içinde gerçekleştirilirse (üst resim), daha düşük yüksekliğe sahip su sütunu hidrojene karşılık gelir, çünkü sıvının yüzeyinde basınç uygulayan daha fazla miktarda gaz vardır. Kabarcıklar elektrotları çevreler ve suyun buhar basıncı geçtikten sonra yükselir.
Tüplerin, bir elektrottan diğerine düşük bir gaz geçişi sağlayacak şekilde birbirlerinden ayrıldığına dikkat edin. Düşük ölçeklerde, bu yakın bir riski temsil etmemektedir; ancak endüstriyel ölçeklerde H'nin gaz karışımı2 ve O2 Çok tehlikeli ve patlayıcı.
Bu nedenle, su elektrolizinin yapıldığı elektrokimyasal hücreler çok pahalıdır; Gazların asla karışmamasını, kârlı bir akım beslemesini, yüksek elektrolit konsantrasyonlarını, özel elektrotları (elektrolizatörler) ve H'yi depolayacak mekanizmaları garanti eden bir tasarıma ve elemanlara ihtiyaç duyarlar2 üretilmiş.
Elektrokatalizörler sürtünmeyi ve aynı zamanda su elektrolizinin karlılığı için kanatları temsil eder. Bazıları, fiyatları çok yüksek olan platin ve iridyum gibi asil metallerin oksitlerinden oluşur. Bu noktada özellikle araştırmacıların verimli, sağlam ve ucuz elektrotların tasarımı için güçlerini birleştirdiği yer.
Bu çabaların nedeni, O oluşumunu hızlandırmaktır.2, H ile karşılaştırıldığında daha düşük hızlarda verilir2. Bu, O'nun oluştuğu elektrot tarafından yavaşlar.2 Genel bir sonuç olarak, gereğinden çok daha büyük bir potansiyelin uygulanmasını sağlar (overpotential); Aynısı nedir, performansı ve masrafları düşürmek için.
indeks
- 1 Elektroliz reaksiyonu
- 1.1 Yarım hücre reaksiyonları
- 2 Prosedür
- 3 Teknik
- 3.1 Alkali su ile elektroliz
- 3.2 Polimer elektrolitik membranlı elektroliz
- 3.3 Katı oksitlerle elektroliz
- 4 Su elektrolizinin kullanımı nedir??
- 4.1 Hidrojen üretimi ve kullanım alanları
- 4.2 Bir hata ayıklama yöntemi olarak
- 4.3 Oksijen kaynağı olarak
- 5 Ev deneyi
- 5.1 Ev değişkenleri
- 6 Kaynakça
Elektroliz reaksiyonu
Suyun elektrolizi, birçok karmaşık yönü içerir. Bununla birlikte, genel anlamda, temeli basit bir küresel tepkidir:
2H20 (l) => 2H2(g) + O2(G)
Denklemde gözlemlendiği gibi, iki su molekülü müdahale eder: biri normalde azaltılmalıdır, ya da elektronlar elde ederken, diğeri elektronları oksitlemeli ya da kaybetmelidir..
H2 Elektronların kazanımı H protonlarını arttırdığından, su azaltma ürünüdür.+ kovalent olarak bağlanabilir ve oksijen OH'ye dönüştürülür-. Bu nedenle, H2 indirgemenin gerçekleştiği elektrot olan katotta meydana gelir.
O iken2 Suyun oksidasyonundan gelir, çünkü hidrojene bağlanmasına izin veren elektronları kaybeder ve sonuç olarak H protonlarını serbest bırakır.+. O2 anotta oksidasyonun meydana geldiği elektrotta meydana gelir; ve diğer elektrotların aksine, anot etrafındaki pH asidiktir ve bazik değildir..
Yarım hücre reaksiyonları
Yukarıdakiler, yarı hücre reaksiyonları için aşağıdaki kimyasal denklemlerle özetlenebilir:
2H2O + 2e- => H2 + 2 OH- (Katot, temel)
2H2O => O2 + 4H+ + 4e- (Anot, asit)
Ancak, su daha fazla elektron kaybedemez (4e-diğer su molekülünün katotta kazandığı (2e)-); bu nedenle, ilk denklemin 2 ile çarpılması ve net denklemin elde edilmesi için ikinci denklemin çıkarılması gerekir:
2 (2 H2O + 2e- => H2 + 2 OH-)
2H2O => O2 + 4H+ + 4e-
6H2O => 2H2 + Ey2 + 4H+ + 4OH-
Ama 4H+ ve 4OH- 4H oluştururlar2Veya bu yüzden bunlar altı H molekülünün dördünü ortadan kaldırır.2Ya da iki tane bırakarak; ve sonuçta ortaya çıkan küresel tepki.
Yarım hücre reaksiyonları, pH değerleri, teknikler ile değişir ve ayrıca suyun elektrolizinin kendiliğinden ilerleyebilmesi için ne kadar akımın sağlanacağını belirleyen potansiyel indirgeme veya oksidasyon potansiyellerine sahiptir..
süreç
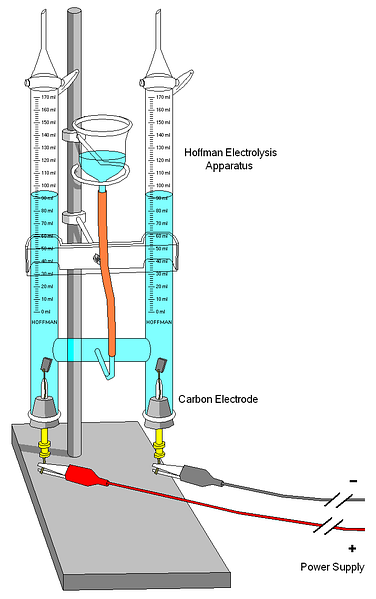
Üstteki resim bir Hoffman voltmetresini gösterir. Silindirler suyla ve seçilen elektrolitlerle orta nozülden doldurulur. Bu elektrolitlerin rolü, suyun iletkenliğini arttırmaktır, çünkü normal koşullar altında çok az H iyonu vardır.3Ey+ ve OH- oto iyonlaştırma ürünleriniz.
İki elektrot genellikle platindir, ancak görüntüde bunların yerine karbon elektrotları kullanılmıştır. Her ikisi de, suyun oksidasyonunu (O oluşumu) destekleyen potansiyel bir farkın (ΔV) uygulandığı bir bataryaya bağlanır.2).
Elektronlar, suyun kazandığı ve H olduğu diğer elektrota ulaşana kadar tüm devreyi dolaşır.2 ve OH-. Bu noktada, anot ve katot hali hazırda tanımlanmış olup, su kolonlarının yüksekliği ile ayırt edilebilir; daha küçük olanı, H'nin oluştuğu katoda karşılık gelir2.
Silindirlerin üst kısmında, üretilen gazları serbest bırakmayı sağlayan bazı anahtarlar vardır. Dikkatlice H varlığını kontrol edebilirsiniz2 yanması gazlı su üreten bir alevle reaksiyona sokulması.
teknikleri
Su elektroliz teknikleri H miktarına bağlı olarak değişir2 ve O2 bu üretmek için teklif edilmiştir. Her iki gaz birlikte karışırlarsa çok tehlikelidir ve bu nedenle elektrolitik hücreler, gaz basınçlarındaki artışı ve sulu ortamdan yayılmalarını en aza indirmek için karmaşık tasarımlar taşırlar..
Aynı zamanda, teknikler hücreye, suya eklenen elektrolite ve elektrotların kendisine bağlı olarak salınır. Öte yandan, bazıları reaksiyonun daha yüksek sıcaklıklarda gerçekleştiğini, elektrik tüketimini azalttığını ve bazılarının H'yi korumak için muazzam baskılar kullandığını ima ediyor2 saklı.
Tüm teknikler arasında aşağıdaki üç söz edilebilir:
Alkali su ile elektroliz
Elektroliz, alkali metallerin (KOH veya NaOH) bazik çözeltileri ile gerçekleştirilir. Bu teknikle reaksiyonlar meydana gelir:
4H2O (l) + 4e- => 2H2(g) + 4OH-(Sulu)
4OH-(ac) => O2(g) + 2H2O (l) + 4e-
Görülebileceği gibi, hem katotta hem de anotta, suyun bazik bir pH'ı vardır; ve ek olarak, OH- O'ya oksitlendikleri anoda göç ederler.2.
Polimer elektrolitik membranlı elektroliz
Bu teknikte H için geçirgen bir zar görevi gören katı bir polimer kullanılır.+, ancak gazlar için su geçirmez. Bu, elektroliz sırasında daha fazla güvenlik sağlar.
Bu durum için yarım hücreli reaksiyonlar:
4H+(ac) + 4e- => 2H2(G)
2H2O (l) => O2(g) + 4H+(ac) + 4e-
H iyonları+ anottan katoda göç ederler, burada H'ye dönüşürler2.
Katı oksitlerle elektroliz
Diğer tekniklerden çok farklı olarak, yüksek sıcaklıklarda (600-900ºC) bir anyon taşıma ortamı olarak işlev gören elektrolitler olarak oksitleri kullanır.2-.
Tepkiler:
2H2O (g) + 4e- => 2H2(g) + 2O2-
2O2- => O2(g) + 4e-
Bu sürenin oksit anyonları, VEYA olduğunu unutmayın.2-, anot için seyahat edenler.
Su elektrolizinin kullanımı?
Su elektrolizi H üretir2 (g) ve O2 (G). Dünyada üretilen hidrojen gazının yaklaşık% 5'i suyun elektrolizi ile üretilmektedir..
H2 sulu NaCl çözeltilerinin elektrolizinin bir yan ürünüdür. Tuz varlığı, suyun elektrik iletkenliğini artırarak elektrolizi kolaylaştırır.
Gerçekleşen küresel tepki:
2NaCl + 2H2O => Cl2 + 'H2 + 2 NaOH
Bu reaksiyonun çok büyük önemini anlamak için, gaz halindeki ürünlerin kullanımlarından bazıları belirtilecektir; çünkü günün sonunda, bunlar su elektrolizini daha verimli ve yeşil bir şekilde elde etmek için yeni yöntemlerin geliştirilmesini sağlayanlardır..
Hepsinden, en çok istenen, yanan fosil yakıtların enerjisel olarak yerini alan hücreler olarak hizmet etmektir..
Hidrojen üretimi ve kullanım alanları
-Elektrolizde üretilen hidrojen, bağımlılık reaksiyonlarında rol oynayan kimya endüstrisinde, hidrojenasyon işlemlerinde veya indirgeme işlemlerinde indirgeyici bir madde olarak kullanılabilir..
-Ayrıca, ticari öneme sahip bazı eylemlerde, örneğin: hidroklorik asit, hidrojen peroksit, hidroksilaminlerin vb. Amonyak sentezinde azot ile katalitik reaksiyona girer.
-Oksijenle birlikte, yüksek kalorili içeriğe sahip, 3.000 ila 3.500 K arasında değişen sıcaklıklarda alevler üretir. Bu sıcaklıklar, metal endüstrisinde kesik ve kaynaklar, sentetik kristallerin büyümesi, kuvars üretimi vb. İçin kullanılabilir..
-Su arıtımı: Sudaki çok yüksek nitrat içeriği, bakterilerin enerji kaynağı olarak hidrojeni kullandıkları biyoreaktörlerde ortadan kaldırılmasıyla azaltılabilir
-Hidrojen plastik, polyester ve naylonun sentezine müdahale eder. Buna ek olarak, pişirme sırasında yanmayı artıran, cam üretiminin bir parçasıdır..
-Aralarında metallerin oksitleri ve kloritleri ile reaksiyona girer, aralarında saf metaller üretmek için gümüş, bakır, kurşun, bizmut ve cıva bulunur.
-Ve ayrıca, bir alev dedektörü ile kromatografik analizlerde yakıt olarak kullanılır..
Bir hata ayıklama yöntemi olarak
Sodyum klorür çözeltilerinin elektrolizi, yüzme havuzu suyunun arıtılması için kullanılır. Elektroliz sırasında, katot ve klorin içinde hidrojen üretilir (Cl2) anotta. Bu durumda, bir tuz klorlama cihazı olarak elektroliz söz konusudur..
Klor suda oluşan hipokloröz asit ve sodyum hipoklorit içinde çözünür. Hipokloröz asit ve sodyum hipoklorit, suyu sterilize eder.
Oksijen kaynağı olarak
Suyun elektrolizi, İstasyondaki bir oksijen atmosferinin korunmasına yarayan Uluslararası Uzay İstasyonunda oksijen üretmek için de kullanılır..
Hidrojen bir yakıt hücresinde, enerjiyi depolamak için bir yöntem ve hücrede üretilen suyu astronotlar tarafından tüketilmek üzere kullanabilir.
Ev deneyi
Hoffman voltmetreleri veya elektrokimyasal bir hücrenin tüm gerekli öğelerini içermesine izin veren başka bir düzeneğe sahip laboratuar ölçeklerinde su elektroliz deneyleri yapılmıştır..
Tüm olası montaj ve ekipmanlardan en basit olanı, bir hücre olarak işlev görecek büyük, şeffaf bir su kabı olabilir. Buna ek olarak, el altında elektrot görevi görebilecek metal veya elektriksel olarak iletken bir yüzeye de sahip olmalısınız; biri katot için diğeri anot için.
Bu amaçla, her iki uçta da bilenmiş grafit uçlu kalemler bile yararlı olabilir. Sonunda küçük bir pil ve onu doğaçlama elektrotlara bağlayan bazı kablolar.
Şeffaf bir kap içinde yapılmazsa, gaz kabarcıklarının oluşumu anlaşılamaz.
Ev değişkenleri
Suyun elektrolizi, alternatif enerji kaynakları arayanlar için ilginç ve umut verici yönleri içeren bir konu olmasına rağmen, ev deneyi çocuklara ve diğer izleyicilere sıkıcı gelebilir..
Bu nedenle, H oluşumunu sağlamak için yeterli voltaj uygulanabilir.2 ve O2 belirli değişkenlerin değiştirilmesi ve değişikliklerin yapılması.
Birincisi, suyun asitlenmesini sağlamak için sirke ya da Na kullanan pH'ın değişimi2CO3 hafifçe bazlaştırmak için. Gözlenen baloncuk miktarında değişiklik olması gerekir.
Ek olarak, aynı deney soğuk ve sıcak su ile tekrarlanabilir. Bu şekilde, sıcaklığın reaksiyon üzerindeki etkisi daha sonra düşünülecektir..
Son olarak, veri toplanmasını biraz daha az renksiz yapmak için, çok seyreltilmiş bir mor lahana suyu çözeltisine başvurabilirsiniz. Bu meyve suyu doğal kökenli bir baz asit göstergesidir..
Kullanılan elektrotlarla kaba eklendiğinde, anotta suyun pembeleşeceği (asit), katotta ise renklenmenin sarı (bazik) olacağı fark edilecektir..
referanslar
- Vikipedi. (2018). Suyun elektrolizi. Alınan: en.wikipedia.org
- Chaplin M. (16 Kasım 2018). Suyun elektrolizi. Su yapısı ve bilimi. Alınan: 1.lsbu.ac.uk
- Enerji Verimliliği ve Yenilenebilir Enerji. (N.D.). Hidrojen üretimi: elektroliz. Alınan kaynak: energy.gov
- Phys.org. (14 Şubat 2018) Su elektrolizi için yüksek verimli, düşük maliyetli katalizör. Alınan: phys.org
- Kimya LibreTexts. (18 Haziran 2015). Suyun elektrolizi. Şu kaynaktan alındı: chem.libretexts.org
- Xiang C., M. Papadantonakisab K. ve S. Lewis N. (2016). Su ayırma için elektroliz sistemlerinin ilkeleri ve uygulamaları. Kraliyet Kimya Derneği.
- Minnesota Üniversitesi'nin bölgeleri. (2018). Suyun Elektrolizi 2. Minnesota Üniversitesi. Şu kaynaktan alındı: chem.umn.edu


