Sodyum Dikromat Özellikleri, Üretimi, Tehlikeleri ve Kullanımları
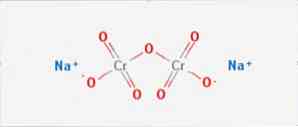
sodyum dikromat Na2Cr2O7 formülüne sahip inorganik bir bileşiktir. Birçok altı değerli krom bileşiğinden (Cr VI) biridir. Yapısı, Şekil 1 'de gösterilmiş olup, genellikle tuzu, Na2Cr2O7 · H20 olacak olan susuz formunda kullanılmasına rağmen.
Sodyum molekülleri ve negatif yüklü oksijenler arasında iki iyonik bağ vardır. Krom cevheri sodyum dikromattan ekstrakte edilir. Yılda milyonlarca kilogram sodyum dikromat üretilir..
Çin, en büyük sodyum dikromat üreticisi olmasına rağmen, Çin kimyasal tesisleri, yıllık 100.000 tondan fazla üretim yapan Kazakistan tesisine kıyasla, her biri yıllık 50.000 tondan daha düşük bir üretime sahip.
Rusya, Amerika Birleşik Devletleri ve Birleşik Krallık'taki tesisler yılda 50.000 ila 100.000 ton arasında bir ara üretime sahiptir (Kogel, 2006).
Reaktivite ve görünüm açısından, sodyum dikromat potasyum dikromata benzer özelliklere sahiptir, ancak sodyum tuzu su içinde daha fazla çözünürdür ve potasyum tuzundan daha az bir ağırlığa eşittir.
Sodyum dikromat ısıtıldığında toksik krom buharları üretir. Güçlü bir oksitleyici ajandır ve çok aşındırıcıdır..
Bu bileşik, galvanizleme veya galvanik kaplama teknikleri, deri tabaklama ve tekstil üretimi gibi farklı endüstriyel işlemlerle kirlenmiş içme suyu kaynaklarında bulunabilir..
indeks
- 1 Fiziksel ve kimyasal özellikler
- 2 Üretim yöntemleri
- 3 Reaktivite ve tehlikeler
- 4 Kullanımlar ve uygulamalar
- 5 Biyokimya
- 6 Kaynakça
Fiziksel ve kimyasal özellikler
Sodyum dikromat susuz ve kokusuz formlarında kırmızımsı turuncu monoklinik yapıya sahip kristallerden oluşur. Moleküler ağırlığı susuz formunda 261.97 g / mol ve susuz formunda 298.00 g / mol'dür.
İçinde parçalandığı 400 derece santigrat kaynama noktasına sahip olan, 356.7 santigrat derece erime noktasına sahiptir. 2.52 g / ml yoğunluğa sahiptir.

Şekil 2, sodyum dikromatın görünümünü göstermektedir. Sudaki çözünürlüğü, 25 derece Santigratta 100 gramda 187 g ve etanolde çözünürlüğü, 19.4 derece Santigrat'da litre başına 513.2 gramdır (Ulusal Biyoteknoloji Bilgi Merkezi, s.)..
Önerilen koşullar altında depolanırsa sabit yanıcı bir bileşik olarak kabul edilir ve yanıcı değildir. Güçlü bir oksitleyici ajan olduğu için, aşındırıcıdır ve çözelti içinde, pH'ı% 4 a / h oranında bir çözeltide pH'ı 4'e düşürme kabiliyetine sahip asittir..
Üretim yöntemleri
Sodyum kromat, sülfürik asit, karbon dioksit veya bu ikisinin bir kombinasyonu ile işlemden geçiren sürekli bir işlemle dikromata dönüştürülebilir..
Sodyum dikromat likörünün buharlaşması, sodyum sülfat ve / veya sodyum bikarbonatın çökelmesine neden olur ve bu bileşikler, sodyum dikromatın nihai kristalizasyonundan önce çıkarılır..
Sodyum dikromat üç aşamalı bir işlemle yapılabilir:
- Kromit oksidasyon koşullarında alkali kavurma
- Liç. Çözünür maddenin bir karışımdan bir sıvı çözücünün etkisiyle çıkarılması
- Bir asit vasıtasıyla sodyum monokromatın sodyum dikromatta dönüşümü.
Susuz sodyum dikromat, sodyum dihidrat dihidratın eritilmesi, sulu dikromat çözeltilerinin 86 ° C'nin üzerinde kristalleştirilmesi veya sodyum kurutucuların sprey kurutucularda kurutulmasıyla hazırlanabilir..
% 69 ve% 70 ağırlık / hacim seviyesinde sodyum dikromat çözeltileri, el ile işleme veya kristallerin çözünmesine gerek kalmadan, miktarların gönderilmesi için uygun ve uygun maliyetli bir yöntem olarak kullanılır..
Tepkime ve tehlikeler
Güçlü bir oksitleyici ajandır. Güçlü asitlerle bağdaşmaz. Yanıcı maddelerle teması yangına neden olabilir. Isı veya ateşin varlığında toksik krom oksit buharları oluşabilir..
Organik artıkları olan dikromat ve sülfürik asidin bilinen "kromik asit karışımı" şiddetli bir ekzotermik reaksiyona neden olur. Aseton kalıntıları ile birlikte bu karışım aynı zamanda şiddetli bir reaksiyona neden olur.
Dikromat ve sülfürik asidin alkoller, etanol ve 2-propanol ile kombinasyonu şiddetli bir ekzotermik reaksiyona neden olur. Dikromat-sülfürik asidin oksitlenebilir organik malzemeler ile karıştırılmasını içeren birçok olayın meydana gelmesi nedeniyle, bu tür etkileşimlerden kaçınmak en iyisidir..
Dikromatın hidrazin ile kombinasyonu patlayıcıdır, dikromat reaksiyonunun genel olarak aminler ile kuvvetli olması beklenebilir. Susuzlaştırılmış dikromat tuzunun asetik anhidride eklenmesi, sonunda patlayıcı bir ekzotermik reaksiyona yol açar.
Bor, silikon ve dikromatlar piroteknik karışımları oluşturur. Asetik asit, 2-metil-2-pentenal ve dikromat karışımı, yaygın bir reaksiyona neden olur (Kimyasal Veri Sayfası Sodyum Dikromat, 2016)..
Tozun veya buğunun solunması bazen astıma benzeyen solunum tahrişine neden olur. Septal perforasyon oluşabilir. Zehir olarak kabul edilir.
Yutulduğunda, kusma, ishal ve çok nadiren mide ve böbrek komplikasyonlarına neden olur. Göz veya cilt ile teması lokal tahrişe neden olur. Cilde tekrar tekrar maruz kalmak dermatite neden olur.
Sodyum dikromat insanlarda kanserojendir. Hekzavalent krom bileşiklerinin veya Cr (VI) 'nın insanlarda akciğer kanserine neden olabileceğine dair kanıt vardır. Sodyum dikromatın hayvanlarda akciğer kanserine neden olduğu gösterilmiştir.
Her ne kadar sodyum dikromat bir teratojenik bileşik veya üreme riski olarak tanımlanmamışsa da, heksavalent krom bileşiklerinin veya Cr (VI) 'nın teratojenik olduğu ve doğurganlığın azaltılması ve adet döngüsüne müdahale etme gibi üreme hasarına neden olduğu bilinmektedir..
Sodyum dikromat karaciğer ve böbrek hasarına neden olabilir, bu nedenle aşırı dikkatle yönetilmesi gerekir (New Jersey Sağlık Bakanlığı, 2009).
Yutulması halinde, mağdur su veya süt içmelidir; asla kusturmaya çalışmayın. Göz veya cilt ile temasında asit yanığı olarak tedavi edilmelidir; Gözlerinizi en az 15 dakika su ile yıkayın..
Dış lezyonlar% 2'lik bir sodyum tiyosülfat çözeltisi ile ovalanabilir. Her durumda bir doktora danışılmalıdır..
Kullanımlar ve uygulamalar
Sodyum dikromat, diğer krom kimyasallarının üretiminde öneminin yanı sıra, aşağıdakilerin üretiminde bir bileşen olarak birçok doğrudan kullanıma sahiptir:
- Metalik yüzey: korozyon direncine yardımcı olur ve metal yüzeyleri temizler, aynı zamanda boyanın yapışmasını kolaylaştırır.
- Organik ürünler: K vitamini ve balmumu gibi ürünlerin imalatında oksitleyici ajanlar olarak kullanılır..
- Pigmentler: ışığa dayanıklı bir renk yelpazesi ürettiği inorganik kromat pigmentlerinin imalatında kullanılır. Bazı kromat dereceleri ayrıca alt katlarda ve primerlerde korozyon önleyici olarak kullanılır..
- Seramik: renkli cam ve seramik camların hazırlanmasında kullanılır.
- Tekstil: hızlı renklendirme özelliklerini geliştirmek için asitli boyalar için mordan olarak kullanılır.
- Krom sülfat üretimi.
(Sodyum dikromat, hemen hemen tüm diğer krom bileşikleri için yapı taşı., 2010-2012)
Sodyum dikromat Dihidrat, kullanımı seramik camlar ve renkli cam gibi yüksek sıcaklık uygulamaları dahil çeşitli koşullarda idealdir.
Titanyum veya demir gibi diğer metal oksitlerden daha sert olan krom oksit, sıcaklık ve proses koşullarının agresif olduğu ortamlar için idealdir..
Bu madde esas olarak diğer krom bileşikleri üretmek için kullanılır, fakat aynı zamanda yağ üretiminde, odun koruyucularda, organik kimyasalların üretiminde ve korozyon önleyici olarak kullanılan bentonit çamurlarında kullanılır..
Alüminyum ve potasyum dikromat ile karıştırıldığında, alümino-termal işlem kullanılarak, kromik oksit yüksek saflıkta metalik krom üretir. Bu, havacılık endüstrisinde kullanılan yüksek performanslı süper alaşımların üretiminde hayati bir bileşendir..
Organik sentezde, sodyum dikromat sülfürik asit varlığında indirgen oksit reaksiyonlarında oksitleyici bir madde olarak kullanılır.
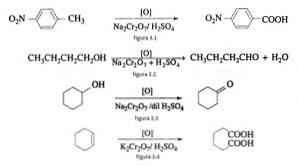
Örneğin, p-nitrotolüenin, p-nitrobenzoik asit oluşturmak için, n-bütanolün, n-bütaldehit oluşturmak üzere, oksloheksanondan sikloheksanon oluşumunda ve Şekil 3.1'de gösterildiği gibi adipik asit oluşumunda oksidasyonu. , Sırasıyla 3.2, 3.3 ve 3.4 (VK Ahluwalia, 2004).
biokimya
Erkek sıçanlarda sodyum dikromat (CrVI) ve krom asetat hidroksitin (CrIII) intratrakeal yerleşimi maruziyetten 72 saat sonra tam kan, plazma ve idrarda krom konsantrasyonlarının artmasına neden oldu; Maruz kalmadan 6 saat sonra maksimum konsantrasyonlara ulaşıldı.
Tam kan krom ve plazma krom konsantrasyonları arasındaki oran, Cr (VI) ve Cr (III) tedavileri için önemli ölçüde farklıydı. Bu nedenle, kandaki krom ve plazmadaki krom analizleri, krom maruziyetinin değerlendirilmesinde kullanılmalıdır..
Periferik lenfositlerde de krom saptandı. Cr (VI), ancak Cr (III) değil, tedaviden sonra lenfositlerde önemli miktarda birikmiştir. Bu hücreler, krom bileşiklerine maruz kalma değerlendirmesinde biyobelirteçler olarak kullanılma potansiyeline sahiptir (Hooth, 2008).
referanslar
- Kimyasal Veri Sayfası Sodyum Dikromat. (2016). Cameo kimyasallarından elde edildi: cameochemicals.noaa.
- Hooth, M.J. (2008). Sodyum Dikromat Dihidratının Toksikoloji ve Karsinojenez Çalışmaları Teknik Raporu. ABD Ulusal Sağlık Enstitüsü ABD.
- Kogel, J. E. (2006). Endüstriyel Mineraller ve Kayalar: Emtialar, Piyasalar ve Yedinci baskıyı kullanır. littleton colorado: madencilik, metalurji ve keşif toplumu.
- Ulusal Biyoteknoloji Bilgi Merkezi. (N.D.). PubChem Bileşik Veritabanı; CID = 25408. Pubchem.com adresinden alındı: pubchem.ncbi.nlm.nih.gov.
- New Jersey Sağlık Bakanlığı. (2009, Kasım). tehlikeli madde bilgi kağıdı sodyum dikromat. Nj.gov'dan alındı: nj.gov.
- Sodyum dikromat. Hemen hemen tüm diğer krom bileşikleri için yapı taşı. (2010-2012). Elementis kromundan alınmıştır: elementischromium.com
- K. Ahluwalia, R.A. (2004). Kapsamlı Pratik Organik Kimya: Hazırlıklar ve Kantitatif Analizler. Delhi: Üniversite basını (Hindistan).


